题目内容
等质量的CO2和SO2的物质的量之比为 ,原子数之比为 ,氧原子质量之比为 ,相同条件下的体积之比为 ,密度之比为 .
考点:阿伏加德罗定律及推论
专题:计算题,阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
计算等质量的SO2和CO2的物质的量之比,相同条件下,体积之比等于物质的量之比、密度之比等于相对分子质量之比,每个分子都含有2个O原子,二者含有的氧原子数目之比等于其物质的量之比.
| m |
| M |
解答:
解:等质量的SO2和CO2,设质量均为m,物质的量之比=
:
=11:16;
分子都为三原子分子,则原子数之比等于分子数之比等于物质的量之比,为11:16;
每个分子都含有2个O原子,等质量的SO2和CO2的含有的氧原子数目之比等于其物质的量之比=11:16;
相同条件下,SO2和CO2的体积之比等于其物质的量之比=11:16;
同温同压下,SO2和CO2的密度之比等于其相对分子质量之比=64:44=16:11,
故答案为:11:16;11:16;11:16;11:16;16:11.
| m |
| 64 |
| m |
| 44 |
分子都为三原子分子,则原子数之比等于分子数之比等于物质的量之比,为11:16;
每个分子都含有2个O原子,等质量的SO2和CO2的含有的氧原子数目之比等于其物质的量之比=11:16;
相同条件下,SO2和CO2的体积之比等于其物质的量之比=11:16;
同温同压下,SO2和CO2的密度之比等于其相对分子质量之比=64:44=16:11,
故答案为:11:16;11:16;11:16;11:16;16:11.
点评:本题考查物质的量的相关计算以及阿伏加德罗定律及其推论的有关知识,题目难度不大,注意有关公式的利用.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
设NA为阿伏伽德罗常数,下列说法正确的是( )
| A、电解精炼铜过程中,电路中每通过NA个电子,阳极溶解铜32g |
| B、1L 2mol/L的NH4CI溶液中含NH4+数目为2NA |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
| D、1molC20H42的分子中含有的共价键数目为61NA |
二维平面晶体所表示的化学式为AX2的是( )
A、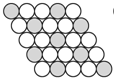 |
B、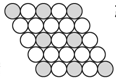 |
C、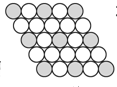 |
D、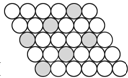 |
由X、Y两元素组成的气态化合物XY4,在一定条件下完全分解为A、B两种气体物质,己知标准状况下20mL XY4分解可产生标准状况下30mL A气体(化学式为Y2)和10mL B气体,则B的化学式为( )
| A、X2 |
| B、Y2X2 |
| C、XY2 |
| D、X2Y4 |
下列说法中正确的是( )
| A、H2SO4的摩尔质量是 98 g |
| B、1 mol H2O的质量是 18 g/mol |
| C、Cl-的摩尔质量是 35.5 g/mol |
| D、1 mol N2 的体积是 22.4 L |
下列离子方程式表达正确的是( )
| A、HCO3-的水解方程式可表示为:HCO3-+H2O═H3O++CO32- |
| B、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| C、向NaAlO2溶液中通入过量的CO2制Al(OH)3↓2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| D、将16g铁粉投入100mL 4.0mol/L的HNO3溶液中,(还原产物只有NO)3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
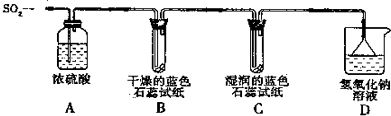
用下列装置进行实验能达到相应实验目的是( )
A、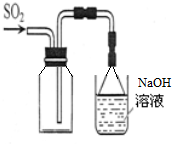 收集SO2气体 |
B、 检验产生的C2H4 |
C、 除去Fe2O3中的Fe(OH)3 |
D、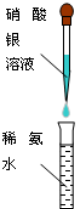 配制银氨溶液 |