题目内容
用下列装置进行实验能达到相应实验目的是( )
A、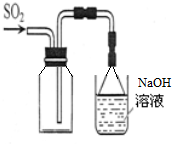 收集SO2气体 |
B、 检验产生的C2H4 |
C、 除去Fe2O3中的Fe(OH)3 |
D、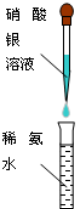 配制银氨溶液 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.根据二氧化硫的密度判断;
B.检验乙烯,应排除乙醇的影响;
C.加热固体,在坩埚中进行;
D.配制银氨溶液,应在硝酸银中滴加氨水.
B.检验乙烯,应排除乙醇的影响;
C.加热固体,在坩埚中进行;
D.配制银氨溶液,应在硝酸银中滴加氨水.
解答:
解:A.二氧化硫的密度比空气大,应用向上排空法收集,故A错误;
B.乙醇易挥发,可与酸性高锰酸钾发生氧化还原反应,检验乙烯,应排除乙醇的影响,故B错误;
C.加热固体,在坩埚中进行,故C正确;
D.配制银氨溶液,应在硝酸银中滴加氨水,注意氨水不能加入过多,至沉淀恰好完全溶解为止,故D错误.
故选C.
B.乙醇易挥发,可与酸性高锰酸钾发生氧化还原反应,检验乙烯,应排除乙醇的影响,故B错误;
C.加热固体,在坩埚中进行,故C正确;
D.配制银氨溶液,应在硝酸银中滴加氨水,注意氨水不能加入过多,至沉淀恰好完全溶解为止,故D错误.
故选C.
点评:本题考查较为综合,涉及气体的收集、检验、固体分解以及溶液的配制等知识,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
已知热化学方程式C2H2(g)+
O2(g)═2CO2(g)+H2O(g)△H=-1256kJ/mol,下列说法正确的是( )
| 5 |
| 2 |
| A、乙炔(C2H2)的燃烧热为1256 kJ/mol |
| B、若转移10 mol电子,则消耗2.5 mol O2 |
| C、若生成2 mol液态水,则△H=-2512 kJ/mol |
| D、若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
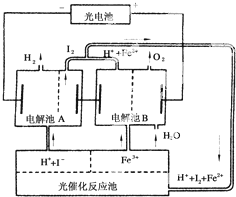 利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如下图所示的循环系统实验光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用.
利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如下图所示的循环系统实验光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用.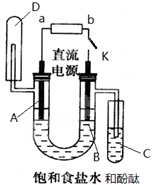 某实验兴趣小组利用如图装置进行电解饱和食盐水并检验其生成产物的实验,当图中开关K闭合片刻后,试填空:
某实验兴趣小组利用如图装置进行电解饱和食盐水并检验其生成产物的实验,当图中开关K闭合片刻后,试填空: