题目内容
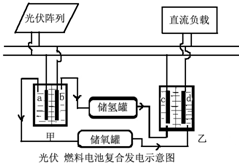 科学家设计出光伏燃料电池发电系统,其工作流程示意图如图:
科学家设计出光伏燃料电池发电系统,其工作流程示意图如图:已知a b c d四个电极均为惰性电极,请根据题意填写下列空白:
(1)甲装置中b为
(2)有下列四种电解质溶液,你认为甲中可以放置:
A.NaCl溶液 B.KOH溶液 C.HCl溶液 D.H2SO4 溶液
(3)根据实际需要,乙装置中可以使用不同的电解质.
①若使用熔融碳酸盐(钠、锂) (650-700℃),写出c电极上反应的电极反应式:
②若使用固体氧化物(Y2O3氧化钇、ZrO2氧化锆,高温下可直接传导O2-),写出c电极上的电极反应式:
(4)已知氢气的燃烧热为:285.8kJ/mol,请写出水电解的热化学方程式:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)乙为氢氧燃料电池,甲为电解池;
(2)甲为电解池,电解时两极上分别生成氢气和氧气,据此判断电解质溶液;
(3)①若使用熔融碳酸盐,则负极上氢气失电子与CO32-结合生成水和二氧化碳;
②若使用固体氧化物,则氢气失电子与O2-结合生成水;
(4)方程式反写时,反应热符号相反,反应热大小与方程式的计量数成正比.
(2)甲为电解池,电解时两极上分别生成氢气和氧气,据此判断电解质溶液;
(3)①若使用熔融碳酸盐,则负极上氢气失电子与CO32-结合生成水和二氧化碳;
②若使用固体氧化物,则氢气失电子与O2-结合生成水;
(4)方程式反写时,反应热符号相反,反应热大小与方程式的计量数成正比.
解答:
解:(1)乙中两极上分别为氢气和氧气反应为氢氧燃料电池,通入氢气的一极为I负极,则c为负极,甲为电解池,b与负极相连为阴极,
故答案为:阴;负;
(2)甲为电解池,电解时两极上分别生成氢气和氧气,
A.若为NaCl溶液,则阳极上生成氯气,不符合条件,故A错误;
B.若为KOH溶液,则阳极上生成氧气,阴极上生成氢气,符合条件,故B正确;
C.若为HCl溶液,则阳极上生成氯气,不符合条件,故C错误;
D.若为H2SO4 溶液,则阳极上生成氧气,阴极上生成氢气,符合条件,故D正确;
故答案为:BD;
(3)①若使用熔融碳酸盐,则负极上氢气失电子与CO32-结合生成水和二氧化碳,则负极上反应的电极反应式:H2-2e-+CO32-=CO2+H2O,
故答案为:H2-2e-+CO32-=CO2+H2O;
②若使用固体氧化物,则氢气失电子与O2-结合生成水,则负极上反应的电极反应式:O2-+H2-2e-=H2O,故答案为:O2-+H2-2e-=H2O;
(4)氢气的燃烧热为:285.8kJ/mol,则氢气燃烧的热化学方程式为:H2(g)+
O2(g)=H2O(l)△H=+285.8kJ/mol,则水电解的热化学方程式为:H2O(l)=H2(g)+
O2(g)△H=+285.8kJ/mol,故答案为:H2O(l)=H2(g)+
O2(g)△H=+285.8kJ/mol.
故答案为:阴;负;
(2)甲为电解池,电解时两极上分别生成氢气和氧气,
A.若为NaCl溶液,则阳极上生成氯气,不符合条件,故A错误;
B.若为KOH溶液,则阳极上生成氧气,阴极上生成氢气,符合条件,故B正确;
C.若为HCl溶液,则阳极上生成氯气,不符合条件,故C错误;
D.若为H2SO4 溶液,则阳极上生成氧气,阴极上生成氢气,符合条件,故D正确;
故答案为:BD;
(3)①若使用熔融碳酸盐,则负极上氢气失电子与CO32-结合生成水和二氧化碳,则负极上反应的电极反应式:H2-2e-+CO32-=CO2+H2O,
故答案为:H2-2e-+CO32-=CO2+H2O;
②若使用固体氧化物,则氢气失电子与O2-结合生成水,则负极上反应的电极反应式:O2-+H2-2e-=H2O,故答案为:O2-+H2-2e-=H2O;
(4)氢气的燃烧热为:285.8kJ/mol,则氢气燃烧的热化学方程式为:H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
点评:本题考查了原电池原理和电解池原理的应用、热化学方程式的书写,注意根据电极上的反应物质判断正负极,把握电解池中阴阳极上离子的放电顺序,题目难度中等.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
下列物质存放方法错误的是( )
| A、金属钠存放于煤油中 |
| B、FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| C、氯水置于棕色试剂瓶避光保存 |
| D、将1mol/L的NaCl溶液保存在容量瓶中 |
下列叙述正确的是( )
| A、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |
| B、两种醋酸溶液的物质的量浓度分别为C1和C2,pH分别为a和a+1,则C1<10 C2 |
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
| D、0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
普通干电池中装有二氧化锰和其他物质,二氧化锰的作用是( )
| A、和正极作用把碳变成CO2 |
| B、把正极附近生成的氢气氧化成水 |
| C、电池中发生化学反应的催化剂 |
| D、和负极作用,将锌变成锌离子Zn2+ |
人的胃液是一种强酸性液体,pH在0.9~1.5之间,氢氧化铝是一种治疗胃酸过多的胃药的主要成分.目前这种胃药已不常用,原因主要是( )
| A、长期摄入铝元素不利于人体健康 |
| B、它不能中和胃液 |
| C、它不易溶于胃液 |
| D、它的疗效太差 |
化学在人类生活中扮演着重要角色,以下应用不正确的是( )
| A、用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
| B、浓硫酸具有吸水性,可用来干燥O2、Cl2、NH3等气体 |
| C、醋可用于除去暖水瓶中的水垢 |
| D、FeCl3可用来制印刷电路板 |
描述或解释下列现象的离子方程式,不正确的是( )
| A、滴有蓝色石蕊的烧碱溶液里通CO2至颜色变红:CO2+2OH-═CO32-+H2O |
| B、稀醋酸溶解水垢中的碳酸钙:2CH3COOH+CaCO3═Ca2++2CH3COO-+H2O+CO2↑ |
| C、碳酸氢铵溶液中加足量石灰水:NH4++HCO3-+Ca2++2OH-═CaCO3↓+NH3?H2O+H2O |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O═Fe(OH)3↓+3HClO |