题目内容
人的胃液是一种强酸性液体,pH在0.9~1.5之间,氢氧化铝是一种治疗胃酸过多的胃药的主要成分.目前这种胃药已不常用,原因主要是( )
| A、长期摄入铝元素不利于人体健康 |
| B、它不能中和胃液 |
| C、它不易溶于胃液 |
| D、它的疗效太差 |
考点:药物的主要成分和疗效
专题:元素及其化合物
分析:Al元素不是人体必需的元素,长期摄入Al元素会引起记忆力下降,易患痴呆症、影响儿童智力发育.
解答:
解:Al元素不是人体必需的元素,长期摄入Al元素会引起记忆力下降,易患痴呆症、影响儿童智力发育等,长期摄入Al元素不利于人体健康;因此不常用Al(OH)3来治疗胃酸过多,是因为服用后生成能被人体吸收的Al3+;
故选A.
故选A.
点评:本题考查了氢氧化铝的性质,及铝元素对人体的危害,注意常见的对人体有害的物质,在选择药品时要将危害降到最低,题目难度不大.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧.下列有关说法不正确的是( )
| A、Na2O2与CO2反应时,Na2O2是氧化剂,CO2是还原剂 |
| B、1mol过氧化钠中阴离子数目为1NA |
| C、过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性 |
| D、过氧化钠与二氧化硫反应时可生成硫酸钠 |
下列有关说法正确的是( )
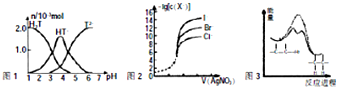

| A、常温下,向20mL 0.1mol?L-1酒石酸(H2T)溶液中添加0.1mol?L-1 NaOH溶液,有关微粒的物质的量与混合溶液的pH关系如图1,则H2T的酸性比H2CO3强 |
| B、用0.0100mol?L-1硝酸根标准溶液,滴定浓度均为0.100mol?L-1的Cl、Br及I的混合溶液,由图2曲线可确定首先沉淀的是Cl- |
| C、碳酸氢钠溶液中存在:c(H+)+2c(H2CO3)=c(OH-)+2c(CO32-) |
| D、由图3可说明烯烃与H2加成反应,虚线表示在催化剂的作用下进行 |
在托盘天平的两个托盘上分别放有同样大小的两个烧杯,烧杯内部分别装有等量盐酸,天平保持平衡.这时,分别向两个烧杯中加入等质量的下列物质,充分反应后(酸过量),天平仍能保持平衡的是( )
| A、CaCO3和KHCO3 |
| B、Na2CO3和NaHCO3 |
| C、Na2CO3和K2CO3 |
| D、Na2CO3和CaCO3 |
据报道,最近国际上研制出了一种新型锂离子电池,该电池的总反应方程式为Li15Si4+15NiO2
4Si+15LiNiO2.下列说法中正确的是( )
| 放电 |
| 充电 |
| A、放电时,电池内部Li+由正极向负极移动 |
| B、每转移0.4 mol电子,有2.8 g Si发生转化 |
| C、放电时负极得电子,质量减轻 |
| D、充电时,阳极的反应式为LiNiO2-e-═NiO2+Li+ |
下列说法都正确的是( )
①江河入海口三角洲的形成通常与胶体的性质有关
②四川灾区重建使用了大量钢材,钢材是合金
③“钡餐”中使用的硫酸钡是弱电解质
④硅的导电性介于导体和绝缘体之间,是良好的半导体材料.
⑤苏打水溶液显碱性,可用其治疗胃胃溃疡患者
⑥明矾可作净水剂.
①江河入海口三角洲的形成通常与胶体的性质有关
②四川灾区重建使用了大量钢材,钢材是合金
③“钡餐”中使用的硫酸钡是弱电解质
④硅的导电性介于导体和绝缘体之间,是良好的半导体材料.
⑤苏打水溶液显碱性,可用其治疗胃胃溃疡患者
⑥明矾可作净水剂.
| A、①②③④ | B、①②④⑥ |
| C、①②⑤⑥ | D、③④⑤⑥ |
能正确表示下列反应的离子方程式是( )
| A、向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
| B、在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2 H2O |
| C、氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O═CaCO3↓+2HClO |
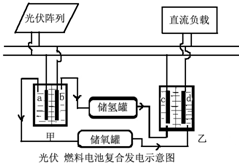 科学家设计出光伏燃料电池发电系统,其工作流程示意图如图:
科学家设计出光伏燃料电池发电系统,其工作流程示意图如图: