题目内容
18.NA代表阿伏加德罗常数的值,下列说法错误的是( )| A. | 2.8g铁与0.05mol Cl2充分反应,转移0.1NA电子 | |
| B. | 27g Al与足量NaOH溶液反应生成 33.6L H2 | |
| C. | 1mol由乙烯(C2H4)和乙烷(C2H6)组成的混合物中含有碳原子的数目为2NA | |
| D. | 0.1mol Na2O2与足量二氧化碳反应转移0.1NA个电子 |
分析 A.2.8gFe的物质的量为0.05mol,0.05molFe完全反应消耗0.15mol氯气,铁过量,0.05mol氯气完全反应得到0.1mol电子;
B.没有告诉在标准状况下,无法计算生成氢气的体积;
C.二者分子中都含有2个C,1mol该混合物中含有2molC原子;
D.0.1mol过氧化钠与二氧化碳完全反应生成0.05mol氧气,结合过氧化钠中氧元素的化合价为-1价计算.
解答 解:A.2.8gFe的物质的量为:$\frac{2.8g}{56g/mol}$=0.05mol,0.05molFe完全反应需要消耗0.15molCl2,说明Fe过量,0.05mol Cl2完全反应得到0.1mol电子,即转移0.1NA电子,故A正确;
B.不是标况下,不能根据标准状况下的气体摩尔体积计算生成氢气的体积,故B错误;
C.1mol由乙烯(C2H4)和乙烷(C2H6)组成的混合物中含有2molC,含有碳原子的数目为2NA,故C正确;
D.0.1mol Na2O2与足量二氧化碳反应生成0.05mol氧气,转移电子的物质的量为0.1mol,转移0.1NA个电子,故D正确;
故选B.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,B为易错点,注意明确标况下气体摩尔体积的使用条件.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
8.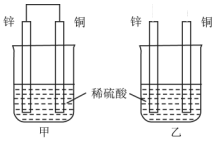 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )
 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 甲中电流由锌片经导线流向铜片 | D. | 两烧杯锌片均发生氧化反应 |
6.除去下列物质中所含的杂质,选用的试剂及方法正确的是( )
| 选项 | 物质(杂质) | 试剂 | 方法 |
| A | CO2(SO2) | 饱和Na2CO3溶液 | 洗气 |
| B | NaCl溶液(Na2CO3) | BaCl2 | 过滤 |
| C | Cl2(HCl) | 饱和NaCl溶液 | 洗气 |
| D | KI溶液(I2) | 乙醇 | 萃取分液 |
| A. | A | B. | B | C. | C | D. | D |
13.下列关于有机化合物的说法正确的是( )
| A. | 利用油脂在酸性条件下水解,可以生产甘油和肥皂 | |
| B. | 合成纤维和人造纤维统称化学纤维 | |
| C. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 淀粉、蛋白质和油脂都属于高分子化合物 |
10.关于如图所示原电池装置的叙述,正确的是( )
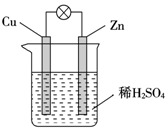

| A. | 电子从铜片经外电路流向锌 | B. | Zn为负极,Cu为正极 | ||
| C. | H+在铜片上得电子发生氧化反应 | D. | 该装置能将电能转化为化学能 |
7.对于反应:N2+3H2?2NH3△H<0,下列叙述正确的是( )
| A. | 升高温度,逆反应速率加快,正反应速率减慢 | |
| B. | 使用催化剂比不使用催化剂化学平衡常数要大 | |
| C. | 由勒夏特列原理可知合成氨时,分离出NH3可以提高原料利用率 | |
| D. | 加压能加快反应速率,因为增加了活化分子百分数 |
8.下列说法中正确的是( )
| A. | Na2S2O3 (aq)+2HCl(aq)=2NaCl(aq)+S(s)+SO2(g)+H2O(l)在加热条件下化学反应速率增大的主要原因是该反应是吸热反应,加热使平衡向正反 应方向移动 | |
| B. | 若在恒容容器中发生反应:N2(g)+3H2(g)?2NH3 (g),达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动 | |
| C. | 在合成氨反应中,其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率一时间图象可用图一表示 | |
| D. | 若在恒压容器中发生反应:2SO3 (g)?2SO2 (g)+O2 (g),达到平衡后再充人适量He,其速率一时间图象可用图二表示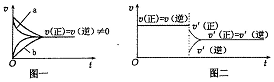 |
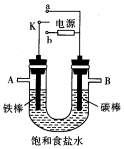 根据如图装置进行电化学的相关实验,回答下列问题.
根据如图装置进行电化学的相关实验,回答下列问题.