题目内容
8.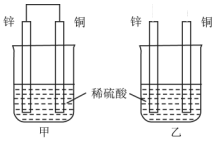 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 甲中电流由锌片经导线流向铜片 | D. | 两烧杯锌片均发生氧化反应 |
分析 由图可知,甲构成原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子生成H2,电池总反应式为:Zn+H2SO4=ZnSO4+H2↑.乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,以此进行分析.
解答 解:A.甲是原电池,正极铜片上发生还原反应 2H++2e-=H2↑,乙装置中在锌片上发生反应 Zn+2H+=Zn2++H2↑,铜片上无气体产生,故A错误;
B.甲装置是原电池,铜片做正极,乙不是原电池,故B错误;
C.甲是原电池,锌作负极,失电子,铜作正极,电流由铜片经导线流向锌片,故C错误;
D.甲是原电池,锌作负极,失电子发生氧化反应,乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,锌片也发生氧化反应,故D正确;
故选:D.
点评 本题考查原电池的有关知识,难度不大,注意把握原电池的构成条件及工作原理,有利于基础知识的巩固.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
19.将某Fe和Al的混合物m g,加入到足量NaOH溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的CuSO4溶液中,充分反应后过滤得到的固体质量仍为m g,则原混合物中Al的质量分数为( )
| A. | 12.5% | B. | 14.3% | C. | 48.2% | D. | 87.5% |
3.下列离子方程式正确的是( )
| A. | 向碳酸氢钙溶液中滴入少量氢氧化钠溶液:OH-+HCO3-+Ca2+═CaCO3↓+H2O | |
| B. | 将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+═Cu+2Na+ | |
| C. | 氢氧化钡溶液与硫酸反应:有白色沉淀生成 Ba2++SO42-═BaSO4↓ | |
| D. | 氯气溶解于水:Cl2+H2O═2H++Cl-+ClO- |
13.据报道,科学家已成功合成了少量N4,有关N4的说法正确的是( )
| A. | N4和N2是氮元素的两种不同单质 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互为同位素 | |
| C. | 相同质量的N4和N2所含原子个数比为1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩尔质量是56g/mol |
20.如果把12C的相对原子质量定义为24,以0.024 kg12C所含的C原子数为阿伏加德罗常数,在标准状况时下列数值肯定不变的是( )
| A. | 浓硫酸(98%)的物质的量浓度 | B. | 常温下氯化钠的溶解度 | ||
| C. | 标准状况下气体摩尔体积 | D. | 0.2g金刚石所含的C原子数 |
17.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Cu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 标准状况下,22.4 L Cl2含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 |
18.NA代表阿伏加德罗常数的值,下列说法错误的是( )
| A. | 2.8g铁与0.05mol Cl2充分反应,转移0.1NA电子 | |
| B. | 27g Al与足量NaOH溶液反应生成 33.6L H2 | |
| C. | 1mol由乙烯(C2H4)和乙烷(C2H6)组成的混合物中含有碳原子的数目为2NA | |
| D. | 0.1mol Na2O2与足量二氧化碳反应转移0.1NA个电子 |
 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.