题目内容
2.下列反应中,属于加成反应的是( )| A. | 苯与液溴在FeBr3催化下生成溴苯 | |
| B. | 乙醇在铜做催化剂的条件下,被空气中的氧气氧化成乙醛 | |
| C. | 乙烯使溴水褪色 | |
| D. | 乙酸与乙醇反应生成乙酸乙酯 |
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,根据定义分析解答.
解答 解:A、苯与液溴在FeBr3催化下生成溴苯,是苯环上的氢原子被溴原子取代,属于取代反应,故A错误;
B、乙醇在铜做催化剂的条件下,被空气中的氧气氧化成乙醛,乙醇分子中H原子数目减少,属于氧化反应,故B错误;
C、乙烯使溴水褪色是乙烯中C=C双键中其中1个碳碳键断裂,不饱和的C原子与溴原子直接结合生成1,2-二溴乙烷,属于加成反应,故C正确;
D、乙酸与乙醇反应生成乙酸乙酯,是乙醇羟基上的氢原子被乙酰基取代生成乙酸乙酯,属于取代反应,故D错误;
故选C.
点评 本题考查有机物的性质,注意加成反应与其它反应类型的区别,题目较为简单.

练习册系列答案
相关题目
12.设NA表示阿伏加德罗常数的数值.下列说法中正确的是( )
| A. | 标准状况下,1 mol SO3的体积为22.4 L | |
| B. | 4 g Ca变成Ca2+失去0.1NA个电子 | |
| C. | 1 mol CH4和1 mol O2质量相等 | |
| D. | 2 g H2中含有2 mol氢原子 |
13.钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源等领域.工业上利用冶炼铝生成的固体废料--赤泥(主要成份为Fe2O3、Al2O3、V2O5及少量稀土金属氧化物)提取金属钒,其工艺流程图如下:

已知:钒有多种价态,其中+5价最稳定.钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O?VO3-+2H+.下列说法正确的是( )

已知:钒有多种价态,其中+5价最稳定.钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O?VO3-+2H+.下列说法正确的是( )
| A. | 工业生产中,碱浸步骤可选用较为廉价的氨水 | |
| B. | 可以推测VO2Cl溶解度大于NH4VO3 | |
| C. | 焙烧非磁性产品所得的固体产物加酸溶解时,应加入过量盐酸以使其溶解完全 | |
| D. | 将磁性产品加入稀硝酸溶解,取上层清液再加入KSCN溶液后未见血红色,则磁性产品中一定不含铁元素 |
17.下列有关煤、石油、天然气等资源的说法正确的是( )
| A. | 石油裂解得到的汽油是纯净物 | B. | 煤就是碳,属于单质 | ||
| C. | 煤的气化是物理变化过程 | D. | 天然气是一种清洁的化石燃料 |
14.下列有关化学用语表示正确的是( )
| A. | CSO的电子式: | |
| B. | 甲烷分子的球棍模型: | |
| C. | 2-戊烯的结构简式CH3CH2CHCHCH3 | |
| D. | HCO3-的水解方程式为:HCO3-+H2O?CO32-+H3O+ |
11.如图是两种烃的球棍模型,有关它们的说法,正确的是( )
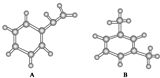

| A. | 两者都能使酸性KMnO4溶液褪色 | B. | 两者都能与溴水反应而使溴水褪色 | ||
| C. | 两者分子中所有原子均可能共平面 | D. | 两者的一氯代物的数目相等 |
3.某工业废水中,除H+、OH-外仅含下表离子中的几种.
甲同学欲探究废水的组成,进行了如下实验:
I.取少量废水样品,加入KSCN溶液无明显变化.
Ⅱ.另取少量废水样品,逐滴加入NaOH溶液,产生沉淀,继续滴加过量的NaOH溶液,沉淀部分溶解.
请回答下列问题:
(1)废水中一定含有的金属阳离子是Al3+Cu2+(填离子符号).
(2)Ⅱ中沉淀部分溶解过程中发生反应的离子方程式是Al(OH)3+OH-=[Al(OH)4]-.
(3)甲同学通过分析最终确定废水中一定不能大量存在上表所列四种阴离子中的CO32-(填离子符号),其判断理由是Al3+与CO32-在水溶液中同时发生水解且两个水解过程相互促进,故废水中不能大量存在CO32-(或Cu2+与CO32-结合生成CuCO3沉淀,故废水中不能大量存在CO32-).
| 阳离子 | Cu2+、Fe3+、Al3+、K+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42- |
I.取少量废水样品,加入KSCN溶液无明显变化.
Ⅱ.另取少量废水样品,逐滴加入NaOH溶液,产生沉淀,继续滴加过量的NaOH溶液,沉淀部分溶解.
请回答下列问题:
(1)废水中一定含有的金属阳离子是Al3+Cu2+(填离子符号).
(2)Ⅱ中沉淀部分溶解过程中发生反应的离子方程式是Al(OH)3+OH-=[Al(OH)4]-.
(3)甲同学通过分析最终确定废水中一定不能大量存在上表所列四种阴离子中的CO32-(填离子符号),其判断理由是Al3+与CO32-在水溶液中同时发生水解且两个水解过程相互促进,故废水中不能大量存在CO32-(或Cu2+与CO32-结合生成CuCO3沉淀,故废水中不能大量存在CO32-).
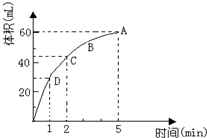 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示,5分钟时反应停止.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示,5分钟时反应停止.请依图回答下列问题: 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置:
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置: