题目内容
13.如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图,下列说法错误的是( )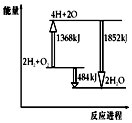
| A. | 拆开2molH2(g)和1molO2(g)中的化学键共吸收1368kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共放出1852kJ能量 | |
| C. | 1molH2(g)和$\frac{1}{2}$molO2(g)反应生成1molH2O(l),放出热量小于242kJ | |
| D. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量 |
分析 由图可知,断裂化学键吸收能量,成键释放能量,且2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量,物质的量与热量成正比,以此来解答.
解答 解:A.由图可知,断裂化学键时,拆开2molH2(g)和1molO2(g)中的化学键共吸收1368kJ能量,故A正确;
B.成键时,由H、O原子形成2molH2O(g),共放出1852kJ能量,故B正确;
C.2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量,物质的量与热量成正比,且气态水的能量高于液态水的能量,则1molH2(g)和$\frac{1}{2}$molO2(g)反应生成1molH2O(l),放出热量大于242kJ,故C错误;
D.由图可知,2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量,故D正确;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、物质的状态为解答的关键,侧重分析与应用能力的考查,注意化学键与能量的关系,题目难度不大.

练习册系列答案
相关题目
16.如图所示装置,其中R为直流电源,以下说法中不正确的是( )


| A. | 若只闭合K1,则铁棒发生的是吸氧腐蚀 | |
| B. | 若要保护铁棒不被腐蚀,则只闭合K2且a极为负极 | |
| C. | 若只闭合K2,一段时间后,U形管中出现白色沉淀,则a极为正极 | |
| D. | 先只闭合K2,两极均产生气体,漏斗液面上升,然后再只闭合K1,漏斗液面不会下降 |
4.能正确表示下列反应的离子方程式的是( )
| A. | Fe3O4溶于足量稀HNO3中:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 将过量的SO2+ClO-+H2O═HClO+HSO3- | |
| D. | 将0.2mol•L-1NH4HCO3溶液与0.3 mol•L-1Ba(OH)2溶液等体积混合:HCO3-+NH4++Ba2++2OH-═NH3•H2O+H2O+BaCO3↓ |
1. 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强P1>P2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强P1>P2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强P1>P2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强P1>P2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )| A. | 上述反应是放热反应 | B. | 上述反应是吸热反应 | ||
| C. | a>b | D. | a+1<b |
8.下列叙述正确的是( )
| A. | 需要加热的反应说明它是吸热反应 | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的稀溶液混合,放出的热量等于57.3 kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
18.下列设计的实验方案不能达到实验目的是( )
| A. | 提纯混有少量硝酸钾的氯化钠采用蒸发结晶,趁热过滤的方法 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入适量饱和Na2CO3溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2 mL 5% H2O2和1 mL H2O,向另一支试管中加2 mL 5% H2O2和1 mL FeCl3溶液,观察并比较实验现象 | |
| D. | 用KI滴定FeCl3溶液时选用淀粉作指示剂 |
5.关于如图所示①、②两个装置的叙述中,正确的是( )


| A. | 硫酸浓度变化:①增大,②减小 | |
| B. | 装置名称:①是原电池,②是电解池 | |
| C. | 电极反应式:①中阳极:4OH--4e-═2H2O+O2↑②中正极:Zn-2e-═Zn2+ | |
| D. | 离子移动方向:①中H+向阴极方向移动,②中H+向负极方向移动 |
3.下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
| A. | SO2+2NaOH═Na2SO3+H2O | B. | 3NO2+2H2O═2HNO3+NO | ||
| C. | 3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | D. | 2Na+2H2O═2NaOH+H2↑ |