题目内容
在氢氟酸溶液中,存在如下电离平衡:HF?H++F-
(1)加入固体NaOH,c(H+) .(填“增大”“减小”“不变”,下同)
(2)加入固体NaF,c(H+) .
(3)升高温度,
.
(1)加入固体NaOH,c(H+)
(2)加入固体NaF,c(H+)
(3)升高温度,
| c(H+) |
| c(HF) |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:在氢氟酸溶液中,存在如下电离平衡:HF?H++F-,升高温度促进弱电解质电离,向弱电解质溶液中加入和氢离子或氟离子反应的物质促进氢氟酸电离,加入含有氢离子或氟离子的物质抑制氢氟酸电离.
解答:
解:(1)加入氢氧化钠固体,氢氧化钠和氢离子反应生成水,促进氢氟酸电离,溶液中氢离子浓度减小,故答案为:减小;
(2)向溶液中加入氟化钠固体,氟离子浓度增大,抑制氢氟酸电离,平衡向逆反应方向移动,溶液中氢离子浓度减小,故答案为:减小;
(3)升高温度,促进氢氟酸电离,平衡向正反应方向移动,氢离子浓度增大,HF的浓度减小,故比值增大,故答案为:增大.
(2)向溶液中加入氟化钠固体,氟离子浓度增大,抑制氢氟酸电离,平衡向逆反应方向移动,溶液中氢离子浓度减小,故答案为:减小;
(3)升高温度,促进氢氟酸电离,平衡向正反应方向移动,氢离子浓度增大,HF的浓度减小,故比值增大,故答案为:增大.
点评:本题考查了弱电解质的电离,明确影响弱电解质电离的因素是解本题关键,难度不大.

练习册系列答案
相关题目
现行的元素周期表的周期数和族数分别是( )
| A、7,18 | B、9,18 |
| C、7,16 | D、9,16 |



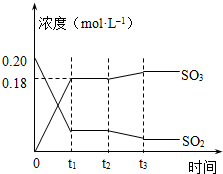 已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示:
已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示: