题目内容
某同学帮助水质检测站配制1000mL 1mol?L-1NaOH溶液以备使用.
(1)该同学应选择 mL的容量瓶.
(2)其操作步骤如下图所示,则如图操作应在下图中的 (填选项字母)之间.

A.②与③B.①与②C.④与⑤
(3)该同学应用托盘天平称取NaOH固体 g,用质量为33.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在下图中选出能正确表示游码位置的选项 (填选项字母).

(4)下列操作对所配溶液的浓度大小有何影响 (填“偏大”、“偏小”或“无影响”).
①定容时,俯视读数,浓度会 ;
②转移溶液过程中,少量液体溅出来,浓度会 ;
③容量瓶未干燥,浓度会 ;
④定容摇匀后发现溶液凹面低于刻度线,浓度会 .
(5)配制溶液的实际操作过程中,动作要快,否则由于 ,会使配制的NaOH溶液的浓度比1mol?L-1 (填“大”或“小”).
(1)该同学应选择
(2)其操作步骤如下图所示,则如图操作应在下图中的

A.②与③B.①与②C.④与⑤
(3)该同学应用托盘天平称取NaOH固体

(4)下列操作对所配溶液的浓度大小有何影响 (填“偏大”、“偏小”或“无影响”).
①定容时,俯视读数,浓度会
②转移溶液过程中,少量液体溅出来,浓度会
③容量瓶未干燥,浓度会
④定容摇匀后发现溶液凹面低于刻度线,浓度会
(5)配制溶液的实际操作过程中,动作要快,否则由于
考点:配制一定物质的量浓度的溶液
专题:实验设计题
分析:(1)选取容量瓶的规格应该等于或稍大于配制溶液的体积;
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在加水振荡与定容之间;
(3)根据m=cVM计算所需的氢氧化钠的质量;游码应在3.1g的位置;
(4)分析操作对溶质的物质的量、溶液体积的影响,根据据c=
分析操作对所配溶液浓度的影响;
(5)根据NaOH易潮解、易吸收空气中的CO2而变质的性质判断.
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在加水振荡与定容之间;
(3)根据m=cVM计算所需的氢氧化钠的质量;游码应在3.1g的位置;
(4)分析操作对溶质的物质的量、溶液体积的影响,根据据c=
| n |
| V |
(5)根据NaOH易潮解、易吸收空气中的CO2而变质的性质判断.
解答:
解:(1)选取容量瓶的规格应该等于或稍大于配制溶液的体积,实验室配制1000mL 1mol?L-1NaOH溶液,所以应该选1000mL容量瓶,故答案为:1000;
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在转移与定容之间,即应在③和④之间,故选:C;
(3)配制1000mL1mol?L-1NaOH溶液需要氢氧化钠的质量为1L×1mol/L×40g/mol=40.0g;
氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯总质量为40.0g+33.1g=73.1g,所以游码应在3.1g的位置,故选择c,
故答案为:40.0;c;
(4)①定容时,俯视读数,溶液体积偏小,配制溶液浓度偏大;
②转移溶液过程中,少量液体溅出来,溶质的物质的量偏小,浓度会偏小;
③容量瓶使用时未干燥,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度无影响;
④定容摇匀后发现溶液凹面低于刻度线,部分溶液附着在瓶壁上,浓度无影响;
故答案为:①偏大②偏小 ③无影响 ④无影响;
(5)配制溶液的实际操作过程中,动作要快,否则由于NaOH易潮解、易吸收空气中的CO2而变质,会使配制的NaOH溶液的浓度比1mol?L-1小,故答案为:NaOH易潮解、易吸收空气中的CO2而变质;小.
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在转移与定容之间,即应在③和④之间,故选:C;
(3)配制1000mL1mol?L-1NaOH溶液需要氢氧化钠的质量为1L×1mol/L×40g/mol=40.0g;
氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯总质量为40.0g+33.1g=73.1g,所以游码应在3.1g的位置,故选择c,
故答案为:40.0;c;
(4)①定容时,俯视读数,溶液体积偏小,配制溶液浓度偏大;
②转移溶液过程中,少量液体溅出来,溶质的物质的量偏小,浓度会偏小;
③容量瓶使用时未干燥,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度无影响;
④定容摇匀后发现溶液凹面低于刻度线,部分溶液附着在瓶壁上,浓度无影响;
故答案为:①偏大②偏小 ③无影响 ④无影响;
(5)配制溶液的实际操作过程中,动作要快,否则由于NaOH易潮解、易吸收空气中的CO2而变质,会使配制的NaOH溶液的浓度比1mol?L-1小,故答案为:NaOH易潮解、易吸收空气中的CO2而变质;小.
点评:本题考查一定物质的量浓度溶液的配制,明确容量瓶规格的选取方法,会根据c=
分析误差,难度不大.
| n |
| V |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质属于电解质的是( )
| A、CO2 |
| B、浓硫酸 |
| C、蔗糖 |
| D、NaCl |
下列离子方程式正确的是( )
| A、Cl2与H2O反应:Cl2+H2O═2H++ClO-+Cl- |
| B、向Na2SiO3溶液中通入过量的CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
| C、向AlCl3溶液中滴加氨水至过量:Al3++3OH-═Al(OH)3↓ |
| D、将铜片投入浓硝酸中:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O |
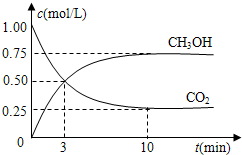 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.