题目内容
15.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 常温常压下,8 g甲烷中含C-H键的数目为4NA | |
| B. | 标准状况下,22.4L乙醇的分子数为NA | |
| C. | 1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA | |
| D. | 标准状况下,16g甲烷分子所含质子数为10NA |
分析 A.甲烷分子中混有个碳氢键,根据n=$\frac{m}{M}$计算出甲烷的物质的量,从而计算出含有的碳氢键数目;
B.标准状况下乙醇不是气体;
C.酯化反应为可逆反应,反应物不可能完全转化成生成物;
D.甲烷分子中含有10个质子,16g甲烷的物质的量为1mol,1mol甲烷中含有10mol质子.
解答 解:A.8g甲烷的物质的量为:$\frac{8g}{16g/mol}$=0.5mol,0.5mol甲烷分子中含有2mol碳氢键,含C-H键的数目为2NA,故A错误;
B.标准状况下,22.4L乙醇物质的量不是1mol,故B错误;
C.1 mol冰醋酸和1mol乙醇经催化加热反应,由于酯化反应为可逆反应,则生成H2O的物质的量一定小于1mol,水分子数小于NA,故C错误;
D.16g甲烷的物质的量=$\frac{16g}{16g/mol}$=1mol,1mol甲烷中含有10mol质子,所含质子数为10NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件.

练习册系列答案
相关题目
5.汽车尾气在光照下,发生光化学烟雾的循环,它的形成过程可用下面的化学方程式表示:NO2$\frac{\underline{\;光\;}}{\;}$NO+O,2NO+O2═2NO2,O+O2═O3.下列叙述中不正确的是( )
| A. | 在此过程中,NO2是氧化剂 | |
| B. | 在此过程中,NO是反应的中间产物 | |
| C. | 该过程总反应的化学方程式为2O3═3O2 | |
| D. | 光化学烟雾能引起人严重的呼吸功能障碍 |
6.相同温度下,将等体、积等pH的醋酸和盐酸溶液,分别加入V1 mL、V2mL的水稀释后,测得溶液的pH仍然相同,则下列关系正确的是( )
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | 无法判断 |
3.物质的量相同的下列有机物,充分燃烧耗氧量最大的是( )
| A. | C2H2 | B. | C2H6 | C. | C4H6 | D. | C4H8 |
10.下列有关化学用语使用正确的是( )
| A. | CO2的电子式: | B. | 氘表示为${\;}_{1}^{2}$D | ||
| C. | S2-离子的结构示意图: | D. | 乙烯的比例模型: |
7.下列反应是吸热反应的是( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
| A. | ①②④ | B. | ②③ | C. | ①④⑤ | D. | ②④ |
5.综合如图判断,下列正确的说法是( )


| A. | 装置I和装置II中负极反应均是Fe-2e-═Fe2+ | |
| B. | 装置I和装置II中正极反应均是O2+4e-+2H2O-═4OH- | |
| C. | 装置I和装置II中盐桥中的阳离子均向右侧烧杯移动 | |
| D. | 装置I和装置II中正极均被保护 |
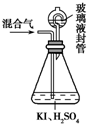 用如图装置可以测定混合气中ClO2的含量:
用如图装置可以测定混合气中ClO2的含量: