��Ŀ����
10��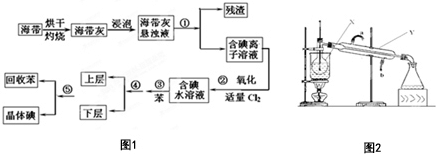 ����ֲ���纣���к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ���ҴӺ�������ȡ�������ͼ��ͼ1������֪��Cl2+2I-�T2Cl-+I2��
����ֲ���纣���к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ���ҴӺ�������ȡ�������ͼ��ͼ1������֪��Cl2+2I-�T2Cl-+I2�� ��1��ָ�����Ĺ������йص�ʵ��������ƣ��ٹ��ˣ�����ȡ���ܷ�Һ��
��2�������ۡ��ܿ��Էֽ�Ϊ���¼�����
A���������������ձ�ʢ����Һ
B���ӷ�Һ©���Ͽڵ����ϲ���Һ
C����Һ©���Ͽڲ�������ʹ���ϵİ��۶�©���Ͽڵ�С��
D�����ã��ֲ�
E����ʢ����Һ�ķ�Һ©����������̨����Ȧ��
F����50mL��ˮ��15mL�������Һ©���У��Ǻò�����
G������Һ©���Ƿ�©Һ
H����ת��Һ©������
��i����ȷ�IJ���˳���ǣ�G��F��H��E��D��C��A��B��
��ii����ѡ�ñ�����ȡ����ԭ���ǣ�����ԭ�ܼ����������Ҳ�������ѧ��Ӧ�����ڱ��е��ܽ��Զ������ˮ�е��ܽ�ȣ�
��iii��������C������������Ŀ���ǣ����ַ�Һ©������ѹ��ƽ�⣬ʹҺ���������£�
��3��������ͼ2�У��������ܺ���ϲ�Һ�壨��ϡ����¡�������ͼ�������в����ݣ�д�����������ƣ�X������ƿ��Y�����ܣ���ָ����ͼװ���д��ڵ�һ�������¶ȼ�ˮ�������뵽Һ�����£�
���� ��1�����������Һ���ù��ˣ���һ���ܼ������ʴ�������һ���ܼ�����ɵ���Һ����ȡ��������ȡ�����������������գ���ˮ���ݣ������˵õ���������Һ����Һ�к��е����ӣ�ͨ����������������ɵ��ˮ��Һ��Ȼ����뱽��ȡ������Һ��õ���ı���Һ���������ɵõ���
��2����i������ȡ����Һ�����������ӷ�Һ©���Ͽڵ����ϲ���Һ��
��ii����ȡ�Ļ���ԭ�������ܼ��������ܣ���������һ���ܼ��е��ܽ�ȱ�����һ�ִ�Ķ࣬��ȡ�������ʲ���Ӧ���ݴ���ѡ����ʵ��Լ�����������ˮ���ҵ��ڱ����ܽ�ȴ���ˮ��
��iii����Һ©���Ͽڲ�������ʹ���ϵİ��۶�©���Ͽڵ�С�ף���ʹ��Һ©������ѹ��ƽ�⣬ʹҺ���������£�
��3�����ܶȱ�ˮС����������װ�÷������������ƣ��¶ȼ�ˮ����Ӧ����ƿ֧�ܿ���ƽ�������¶ȣ�
��� �⣺��1�����������ڲ�����ˮ�Ĺ����Һ�壬���������������գ���ˮ���ݣ������˵õ���������Һ������ˮ�еĵⵥ����ȡ������ѡ����ʵ���ȡ�����ɣ�
���뱽��ȡ������Һ��õ���ı���Һ�������Ϸ�����֪��Ϊ���ˣ���Ϊ��ȡ����Ϊ��Һ��
�ʴ�Ϊ�����ˣ���ȡ����Һ��
��2����i���ۡ���˳��Ϊ������Һ©���Ƿ�©Һ����50mL��ˮ��15mL�������Һ©���У��Ǻò���������ת��Һ©��������ʢ����Һ�ķ�Һ©����������̨����Ȧ�ϡ����ã��ֲ����Һ©���Ͽڲ�������ʹ���ϵİ��۶�©���Ͽڵ�С�ס��������������ձ�ʢ����Һ���ӷ�Һ©���Ͽڵ����ϲ���Һ��������ȷ�IJ���˳���ǣ�GFHEDCAB��
�ʴ�Ϊ��F��H��C��A��B��
��ii������ԭ�ܼ����������Ҳ�������ѧ��Ӧ�����ڱ��е��ܽ��Զ������ˮ�е��ܽ�ȣ���Ӧ���ñ�����ȡ����
�ʴ�Ϊ������ԭ�ܼ����������Ҳ�������ѧ��Ӧ�����ڱ��е��ܽ��Զ������ˮ�е��ܽ�ȣ�
��iii����������Һ���ڴ���ѹ��������������Ŀ���DZ��ַ�Һ©������ѹ��ƽ�⣬ʹҺ���������£�
�ʴ�Ϊ�����ַ�Һ©������ѹ��ƽ�⣬ʹҺ���������£�
��3�������ܶȱ�ˮС�������ϲ㣬�����ܽ�⣬������ߣ���������ķ���������ʱ������װ�ã�XΪ������ƿ��YΪ�����ܣ�Ϊ�������������ˮӦ���¶˽����϶˳����������ƿ�л��գ�װ���д��ڵ�һ�������¶ȼ�ˮ�����λ�ô����¶ȼ�ˮ�������뵽Һ�����£��¶ȼ�ˮ����Ӧ����ƿ֧�ܿ���ƽ�������¶ȣ�
�ʴ�Ϊ���ϣ�������ƿ�������ܣ��¶ȼ�ˮ�������뵽Һ�����£�
���� ���⿼�����ʵķ�����ᴿ��Ϊ��Ƶ���㣬����ѧ���ķ�����ʵ�������Ŀ��飬ѧϰ��ע�����չ��ˡ���ȡ������Ȳ���Ҫ�㣬��Ŀ�Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | �÷�Ӧ���ؼ�С�ķ�Ӧ | |
| B�� | �÷�Ӧ�����ȷ�Ӧ����˲����Է����� | |
| C�� | �жϷ�Ӧ�ܷ��Է�������Ҫ���ݡ�H���S�ۺϿ��� | |
| D�� | ��NH4��2CO3��s����NH4HCO3��s���ȶ� |
 ���������ձ�����һ����Ҫ���ָ����SO2�ĺ����������ѧ֪ʶ�ش��������⣮��ҵ������Ĺ����У�SO2��������ԭ����2SO2��g��+O2��g��$?_{��}^{����}$2SO3��g����H��0
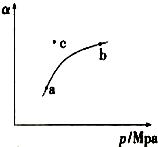
���������ձ�����һ����Ҫ���ָ����SO2�ĺ����������ѧ֪ʶ�ش��������⣮��ҵ������Ĺ����У�SO2��������ԭ����2SO2��g��+O2��g��$?_{��}^{����}$2SO3��g����H��0��1��ij�¶��£����SO2��g����ƽ��ת���ʣ���������ϵ��ѹǿ�� p ���Ĺ�ϵ����ͼ��ʾ��a��b�����Ӧ��ƽ�ⳣ��K��a��= K��b�� ���������������=������ͬ��SO3Ũ��c��a����c��b�� c�㣬��Ӧ���ʦԣ��������ԣ��棩��
��2����һ������SO2��g����O2��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У��ڲ�ͬ�¶��½��У���Ӧ�õ����±��е��������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ||
| SO2 | O2 | SO2 | O2 | ||
| 1 | T1 | 4 | 2 | x | 0.8 |
| 2 | T2 | 4 | 2 | 0.4 | y |
��1������һ��;���ǽ�CO2ת�����л���ʵ��̼ѭ�����磺
2CO2��g��+2H2O��1���TC2H4��g��+3O2��g������H=+1411.0kJ/mol
2CO2��g��+3H2O��1���TC2H5OH��1��+3O2��g����H=+1366.8kJ/mol
������ϩˮ�����Ҵ���Ӧ���Ȼ�ѧ����ʽΪC2H4��g��+H2O��l���TC2H5OH��l����H=-44.2 kJ/mol��
��2����һ�������£�6H2��g��+2CO2��g��?CH3CH2OH��g��+3H2O��g����
�¶ȣ�K�� CO2ת���ʣ�%�� n��H2��/n��CO2�� | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
���¶�һ��ʱ�������̼��[n��H2��/n��CO2��]��CO2��ת���ʣ������������С�������䡱����
�ڸ÷�Ӧ������ӦΪ�ţ�������š����ȷ�Ӧ��
��3��һ�������£���3molH2��lmolCO2�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3H2��g��+CO2��g��?CH3OH��g��+H2O��g���� 2minĩ�÷�Ӧ�ﵽƽ�⣬���
CH3OH��Ũ��Ϊ0.2mol/L�������жϲ���ȷ����bcd
a���������´˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪk=$\frac{c��C{H}_{3}OH��•c��{H}_{2}O��}{{c}^{3}��{H}_{2}��•c��C{O}_{2}��}$
b��H2��ƽ����Ӧ����Ϊ0.3mol/��L•s��
c��CO2��ת����Ϊ60%
d�����������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬
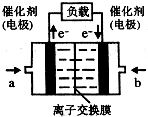
��4����ͼ���Ҵ�ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����a��ͨ������Ҵ�����Ҵ���������������b���缫�Ϸ����ĵ缫��Ӧ�ǣ�O2+4e-+2H2O=4OH-��
��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ����1.4��10-5mol/L��
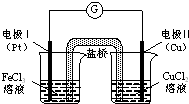
| A�� | �缫���Ϸ�����ԭ��Ӧ����ԭ��ص����� | |
| B�� | �缫��ĵ缫��ӦʽΪ��Cu-2e-�TCu2+ | |
| C�� | ��ԭ��ص��ܷ�ӦΪ��2Fe3++Cu�TCu2++2Fe2+ | |
| D�� | ������װ�к��Ȼ��ص���֬���������Ǵ��ݵ��� |
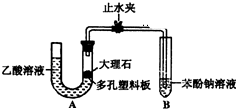 ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮̽�����ᡢ̼��ͱ��ӵ�����ǿ����ϵ��Уѧ���������ͼ��ʵ��װ�ã��г���������ȥ����
ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮̽�����ᡢ̼��ͱ��ӵ�����ǿ����ϵ��Уѧ���������ͼ��ʵ��װ�ã��г���������ȥ���� -ONa��Һ��pH����pH�ɴ�С���е�˳��Ϊbdac��������Һ��ţ�
-ONa��Һ��pH����pH�ɴ�С���е�˳��Ϊbdac��������Һ��ţ�