题目内容
19.如图是某同学设计的原电池装置,下列叙述中不正确的是( )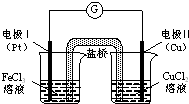
| A. | 电极Ⅰ上发生还原反应,作原电池的正极 | |
| B. | 电极Ⅱ的电极反应式为:Cu-2e-═Cu2+ | |
| C. | 该原电池的总反应为:2Fe3++Cu═Cu2++2Fe2+ | |
| D. | 盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
分析 该原电池中,铜电极易失电子发生氧化反应而作负极,铂电极上铁离子得电子发生还原反应,则铂电极是正极,盐桥的作用是平衡正负极两池的电荷,以此解答该题.
解答 解:A.铂电极上铁离子得电子发生还原反应,所以铂电极作正极,故A正确;
B.铜电极上铜失电子发生氧化反应,电极反应式为:Cu-2e-═Cu2+,故B正确;
C.该原电池负极上铜失电子,正极上铁离子得电子,所以其电池反应式为2Fe3++Cu═Cu2++2Fe2+,故C正确;
D.盐桥的作用是平衡正负极两池的电荷,盐桥中离子的定向移动形成电流,故D错误;
故选D.
点评 本题考查原电池原理,为高频考点,侧重于学生的分析能力的考查,明确正负极上得失电子是解本题关键,知道盐桥的作用,注意电子不进入电解质溶液和盐桥中,为易错点,学习中注意把握原电池的工作原理以及电极方程式的书写和分析.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
10.一定条件下,密闭容器中可逆反应:X(g)+Y(g)?Z(g)+W(s):△H>0 已达平衡下列叙述正确的是( )
| A. | 保持其它条件不变,加入少量W,平衡将逆向移动 | |
| B. | 保持温度和体积不变,加入少量X,正、逆反应速率均增大 | |
| C. | 保持体积不变,升高温度,正反应速率增大,逆反应速率降低 | |
| D. | 保持温度不变,将体积压缩一半,新平衡时体系压强变为原来的两倍 |
7.铜锌原电池(如图)工作时,下列叙述正确的是( )
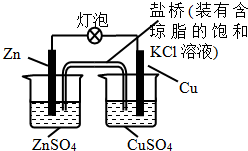

| A. | 一段时间后,铜棒上有红色物质析出 | |
| B. | 正极反应为:Zn-2e-=Zn2+ | |
| C. | 在外电路中,电流从锌棒流向铜棒 | |
| D. | 盐桥中的K+移向ZnSO4溶液 |
4.下列有关化学用语表示正确的是( )
| A. | Cl-的结构示意图: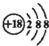 | |
| B. | NaClO的电子式: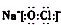 | |
| C. | 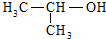 的名称:2-甲基乙醇 的名称:2-甲基乙醇 | |
| D. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{78}$ I |
11. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成Cu而使Cu2O产率降低.
(2)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O
(3)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;\;\;光\;\;\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0
水蒸气的浓度(mol•L-1)随时间t (min)变化如下表:
可以判断:实验①的前20 min的平均反应速率 ν(O2)=3.5×10-5mol/(L.min);;实验温度T1<T2(填“>”“<”);催化剂的催化效率:实验①<实验②(填“>”、“<”).
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(2)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O
(3)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;\;\;光\;\;\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0
水蒸气的浓度(mol•L-1)随时间t (min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
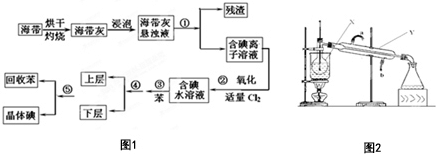 海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海带中提取碘的流程图如图1:(已知:Cl2+2I-═2Cl-+I2)
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海带中提取碘的流程图如图1:(已知:Cl2+2I-═2Cl-+I2) 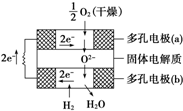 2010年10月上海世博会临近结束的时刻,燃料电池车成为世博会上冉冉升起的新星.燃料电池是一种新型电池,它主要是利用燃料在氧化过程中把化学能直接转化为电能.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,它已用于宇宙飞船及潜艇中.
2010年10月上海世博会临近结束的时刻,燃料电池车成为世博会上冉冉升起的新星.燃料电池是一种新型电池,它主要是利用燃料在氧化过程中把化学能直接转化为电能.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,它已用于宇宙飞船及潜艇中.