题目内容
13.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )| A. | 将NaHCO3固体加入新制氯水,有无色气泡生成(H+) | |
| B. | 使红色布条褪色(HClO) | |
| C. | 向NaBr溶液中滴加氯水,再滴加CCl4,发现下层为橙红色(HCl) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
分析 氯气与水反应,发生Cl2+H2O=H++Cl-+HClO,氯水中含有HClO、Cl2,具有氧化性,其中HClO具有漂白性,含有H+,具有酸性,以此解答.
解答 解:A.氯水显酸性,氯气和水反应生成元素和次氯酸,盐酸能与碳酸氢钠反应生成CO2气体,故A不选;
B.次氯酸具有强氧化性,能氧化有色布条,故B不选;
C.向NaBr溶液中滴加氯水,是氯气氧化了溴离子为Br2,再滴加密度大于水的CCl4,发现下层为橙红色,与HCl无关,故C选.
D.氯离子和硝酸银反应生成氯化银白色沉淀,故D不选;
故选C.
点评 本题考查氯气的性质,侧重于氯水的组成和性质的考查,为高频考点,难度中等,注意把握相关物质的性质.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
3.很长一段时间认为不存在+7价的溴化合物,直到1968年Appolaman利用下列反应:XeF2+HBrO3+H2O→HBrO4+Xe↑+2HF,首次得到此类化合物.在该反应中作还原剂的物质是( )
| A. | HBrO3 | B. | XeF2 | C. | HBrO4 | D. | Xe |
8.以下是人们对原子结构的认识所经历的几个重要历史阶段:
①道尔顿提出的原子论;②汤姆孙提出的葡萄干面包原子模型;
③古希腊哲学家德谟克里特的古典原子论;④卢瑟福的原子结构行星模型.
其中先后顺序正确的是( )
①道尔顿提出的原子论;②汤姆孙提出的葡萄干面包原子模型;
③古希腊哲学家德谟克里特的古典原子论;④卢瑟福的原子结构行星模型.
其中先后顺序正确的是( )
| A. | ①③②④ | B. | ③②①④ | C. | ③①④② | D. | ③①②④ |
18.下列物质,不能由金属单质和稀盐酸反应得到的是( )
| A. | FeCl2 | B. | CuCl2 | C. | AlCl3 | D. | ZnCl2 |
5.物质的量分别为1mol的下列微粒中,具有相同电子总数的一组微粒是( )
| A. | K+和Na+ | B. | Al3+和Cl- | C. | OH-和NH4+ | D. | H2S和CH4 |
7.铁及其化合物在日常生活、生产中应用广泛.
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的.按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3X+5H2O,则X的化学式NaCl.
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
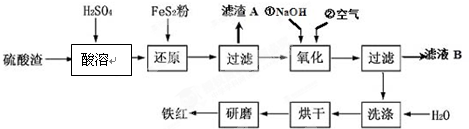
①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
“滤渣A”主要成份的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+.
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,如果pH过大,可能引起的后果是Al3+、Mg2+形成沉淀,使制得的铁红不纯(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式)Na2SO4、Al2(SO4)3、MgSO4.
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的.按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3X+5H2O,则X的化学式NaCl.
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
“滤渣A”主要成份的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+.
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,如果pH过大,可能引起的后果是Al3+、Mg2+形成沉淀,使制得的铁红不纯(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式)Na2SO4、Al2(SO4)3、MgSO4.
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |