题目内容
6.下列物质的变化中,发生了氧化反应的是( )| A. | MnO4-→Mn2+ | B. | H2S→SO2 | C. | CuO→Cu | D. | Fe3+→Fe2+ |
分析 发生了氧化反应,则为还原剂的氧化反应,还原剂中某元素的化合价升高,以此来解答.
解答 解:A.Mn元素的化合价降低,发生还原反应,故A不选;
B.S元素的化合价升高,发生氧化反应,故B选;
C.Cu元素的化合价降低,发生还原反应,故C不选;
D.Fe元素的化合价降低,发生还原反应,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的分析,题目难度不大.

练习册系列答案
相关题目
16.下列叙述正确的是( )
| A. | 生铁中含有碳,抗腐蚀能力比纯铁强 | |
| B. | 钢铁发生析氢腐蚀时,负极反应是:Fe-3e-═Fe3+ | |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| D. | 铁管上镶嵌锌块,铁管不易被腐蚀 |
14.下列有关说法正确的是( )
| A. | 实验室制氢气,为了加快反应速率,可向稀 H2SO4 中滴加少量 Cu(NO3)2 溶液 | |
| B. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变升高温度,平衡时氢气转化率增大 | |
| C. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的△S<0 | |
| D. | 为处理锅炉水垢中的 CaSO4,可先用饱和 Na2CO3 溶液浸泡,再加盐酸溶解 |
18.胶体区别于其它分散系的本质特征是( )
| A. | 胶体稳定 | B. | 胶体有丁达尔效应 | ||
| C. | 胶体能净水 | D. | 胶粒直径在1-100nm之间 |
15.下列说法正确的是( )
| A. | 元素的单质一定是由还原该元素的化合物来制得 | |
| B. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
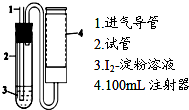 二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:
二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:




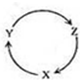 下表各组物质中,满足下右图物质一步转化关系的选项是( )
下表各组物质中,满足下右图物质一步转化关系的选项是( )