题目内容
13.下列有机反应类型判断不正确的是( )| A. | ClCH2CH2Cl+2CH3NH2→CH3NHCH2CH2NHCH3+2HCl 取代反应 | |
| B. |  +CH${\;}_{{\;}_{3}}$CH2OH→ +CH${\;}_{{\;}_{3}}$CH2OH→ 加成反应 加成反应 | |
| C. | HOCH2CH2CH2OH$\stackrel{浓硫酸}{→}$ +H2O消去反应 +H2O消去反应 | |
| D. | nCH2=O$\stackrel{一定条件}{→}$ 加聚反应 加聚反应 |
分析 A.氨基中H被-Cl取代;
B.C=O键转化为单键;
C.分子之间脱水生成环醚,为取代反应;
D.甲醛中含碳氧双键,发生加聚反应生成高分子.
解答 解:A.氨基中H被-Cl取代,则该反应为取代反应,故A正确;
B.C=O键转化为单键,则该反应为加成反应,故B正确;
C.分子之间脱水生成环醚,为取代反应,而不是消去反应,故C错误;
D.甲醛中含碳氧双键,发生加聚反应生成高分子,为加聚反应,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的性质、有机反应等为解答的关键,侧重分析与应用能力的考查,注意官能团与性质的关系,题目难度不大.

练习册系列答案
相关题目
3.在一定温度下的定容容器中,发生反应:2A(g)+B(s)?C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的压强不变②混合气体的密度不变③B 的物质的量浓度不变
④容器内A的百分含量为20%的状态 ⑤单位时间内生成n molD,同时生成2n molA.
⑥单位时间内生成n molC,同时消耗n molD.
①混合气体的压强不变②混合气体的密度不变③B 的物质的量浓度不变
④容器内A的百分含量为20%的状态 ⑤单位时间内生成n molD,同时生成2n molA.
⑥单位时间内生成n molC,同时消耗n molD.
| A. | ②⑤⑥ | B. | ③④⑥ | C. | ①②③ | D. | 只有③ |
4.下列有机物分子中,在质子核磁共振谱中只给出一种峰(信号)的是( )
| A. | CH3OH | B. | CH3COOCH3 | C. | C(CH3)4 | D. | CH3COOH |
1.已知25℃、101kPa下,下列反应
C(石墨)+O2(g)═CO2(g),△H=-393.51kJ
C(金刚石)+O2(g)═CO2(g),△H=-395.41kJ
可以得出的正确结论是( )
C(石墨)+O2(g)═CO2(g),△H=-393.51kJ
C(金刚石)+O2(g)═CO2(g),△H=-395.41kJ
可以得出的正确结论是( )
| A. | 石墨的能量比金刚石低 | B. | 石墨和金刚石都是碳的同位素 | ||
| C. | 金刚石转变为石墨是物理变化 | D. | 金刚石比石墨更稳定 |
8.柠橡烯是一种食用香料,其结构为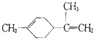 ; 有关柠檬烯的分析正确的是( )
; 有关柠檬烯的分析正确的是( )
 ; 有关柠檬烯的分析正确的是( )
; 有关柠檬烯的分析正确的是( )| A. | 柠檬烯的一氯代物有9种 | |
| B. | 柠檬烯和丁基苯 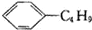 互为同分异构体 互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | -定条件下,柠檬烯可以发生取代反应和氧化反应 |
18.某烃含有一个碳碳三键,与氢气发生加成反应后,产物结构简式为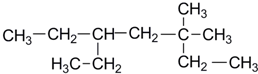 ,则该烃的可能的结构有几种( )
,则该烃的可能的结构有几种( )
 ,则该烃的可能的结构有几种( )
,则该烃的可能的结构有几种( )| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
5.50℃时的KCl饱和溶液,降低10℃,下列因素不发生变化的是( )
| A. | 溶解度 | B. | 溶质的质量分数 | C. | 溶剂的质量 | D. | 溶液的质量 |