题目内容
1.已知25℃、101kPa下,下列反应C(石墨)+O2(g)═CO2(g),△H=-393.51kJ
C(金刚石)+O2(g)═CO2(g),△H=-395.41kJ
可以得出的正确结论是( )
| A. | 石墨的能量比金刚石低 | B. | 石墨和金刚石都是碳的同位素 | ||
| C. | 金刚石转变为石墨是物理变化 | D. | 金刚石比石墨更稳定 |
分析 根据石墨、金刚石燃烧的热化学方程式,利用盖斯定律写出金刚石与石墨转化的热化学方程式,根据反应热比较金刚石与石墨的能量大小.
解答 解:由石墨、金刚石燃烧的热化学方程式①C(石墨)+O2(g)=CO2(g)△H=-393.51kJ•mol-1
②C(金刚石)+O2(g)=CO2(g)△H=-395.41kJ•mol-1,
利用盖斯定律将①-②可得:C(石墨)=C(金刚石);△H=+1.9kJ•mol-1,则
A.通过计算得知:石墨的能量比金刚石低,故A正确;
B.石墨和金刚石均是碳元素形成的不同种单质,互为同素异形体,故B错误;
C.有新物质生成的变化是化学变化,故C错误;
D.能量越低越稳定,石墨稳定,故D错误,
故选A.
点评 本题考查热化学方程式的书写及应用,题目难度不大,注意吸热反应与反应物和生成物能量的关系.

练习册系列答案
相关题目
12.可逆反应2NO 2?2NO+O 2在恒容密闭容器中反应,可以作为达到平衡状态的标志是( )
| A. | 单位时间内生成n mo1 O2的同时生成2n mol NO2 | |
| B. | 单位时间内生成n mol O2的同时生成2n mol NO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的密度不再改变的状态 |
9.X、Y、Z、W、R是短周期中的五种元素,其原子序数依次增大,X、W最外层电子数相等,X为地壳中含量最多的元素,Y是短周期中金属性最强的元素,Z单质是生活应用广泛的常见金属单质,下列说法不正确的是( )
| A. | 原子半径:Y>X | B. | 最高价氧化物的水化物的酸性:R>W | ||
| C. | 气态氢化物的稳定性:X>W | D. | 单质与水(或酸)反应的剧烈程度:Z>Y |
6.下列化学用语正确的是( )
| A. | CH4的比例模型: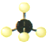 | B. | 乙醇的结构简式C2H6O | ||
| C. | 乙炔分子式:HC≡CH | D. | 丙酸的键线式: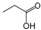 |
13.下列有机反应类型判断不正确的是( )
| A. | ClCH2CH2Cl+2CH3NH2→CH3NHCH2CH2NHCH3+2HCl 取代反应 | |
| B. |  +CH${\;}_{{\;}_{3}}$CH2OH→ +CH${\;}_{{\;}_{3}}$CH2OH→ 加成反应 加成反应 | |
| C. | HOCH2CH2CH2OH$\stackrel{浓硫酸}{→}$ +H2O消去反应 +H2O消去反应 | |
| D. | nCH2=O$\stackrel{一定条件}{→}$ 加聚反应 加聚反应 |
10.下表中,对有关除杂的方法不正确的是( )
| 物质 | 杂质 | 方法 | |
| A | 乙烷 | 乙烯 | 一定条件下与H2反应使乙烯转化为乙烷 |
| B | 乙炔 | H2S | 通入CuSO4溶液的洗气瓶洗气 |
| C | 溴苯 | Br2 | 加NaOH溶液后分液 |
| D | 工业酒精 | H2O(转为无水酒精) | 加入生石灰,蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
5.某学习研究小根据金属锌、铝、铁分别与稀盐酸反应的相对速率,探究金属锌、铝、铁的金属活动性和反应速率测定.
【实验设计】为了达到实验目的,必须控制实验条件.你认为控制的实验条件是(可填满也可不填满)
(1)反应体系的温度(相同);(2)盐酸的浓度(相同);(3)取用盐酸的体积(相同);(4)金属的(比)表面积(或金属粉末的粗细程度)(相同).
【实验探究】该学习研究小组在上述实验条件相同的情况下,进行三组实验:各量取50mL稀盐酸于小烧杯中,分别同时加入足量的三种表面无氧化膜的金属片,用pH计测定溶液的pH并将信息传输到电脑,电脑动态地绘制出溶液中c(H+)随时间t的变化曲线(反应过程中溶液的体积没有变化).图1是反应到t1s时电脑记录的曲线:
【交流与表达】根据上述c(H+)随时间t的变化曲线回答下列问题: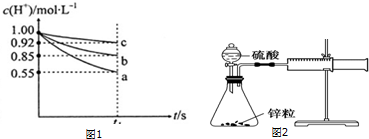
(1)表示金属活动性最弱的金属与H+反应的变化曲线是c(填“a”、“b”或“c”编号).
(2)在同一时间内,表示不同反应的反应速率可以有:同温同压下放出氢气的体积V(H2);溶液中H+浓度的减少△c(H+);固体减少的量△m或△n.在0一t1s之间,设A1和Zn分别与盐酸反应的速率为v(Al)和v(Zn):
Ⅰ.若以溶液中c(H+)减少来表示不同反应的速率,即v(Al):v(Zn)═3:1;
Ⅱ.若以固体质量的减轻来表示不同反应的速率,即v(Al):v(Zn)═54:65;
Ⅲ.若以固体物质的量减少来表示不同反应的速率,即v(Al):v(Zn)═2:1.
IV.可以利用图2所示的装置测定不同浓度的硫酸与锌的反应速率,请回答下列问题:
按照上述装置图安装3套相同的装置,并检验装置气密性良好,将注射器的活栓推至“0”刻度处;然后在三个锥形瓶中分别放入相同形状的锌粒2g,并分别通过分液漏斗在锥形瓶中加入1mol•L-1、2mol•L-1和4mol•L-1的稀硫酸40mL.请补全下表空白:
请选择一组合适的数据填写在第②组实验中的a、b处B.
A.12和0.83B.6和1.67C.1和10D.6和3.67.
【实验设计】为了达到实验目的,必须控制实验条件.你认为控制的实验条件是(可填满也可不填满)
(1)反应体系的温度(相同);(2)盐酸的浓度(相同);(3)取用盐酸的体积(相同);(4)金属的(比)表面积(或金属粉末的粗细程度)(相同).
【实验探究】该学习研究小组在上述实验条件相同的情况下,进行三组实验:各量取50mL稀盐酸于小烧杯中,分别同时加入足量的三种表面无氧化膜的金属片,用pH计测定溶液的pH并将信息传输到电脑,电脑动态地绘制出溶液中c(H+)随时间t的变化曲线(反应过程中溶液的体积没有变化).图1是反应到t1s时电脑记录的曲线:
【交流与表达】根据上述c(H+)随时间t的变化曲线回答下列问题:

(1)表示金属活动性最弱的金属与H+反应的变化曲线是c(填“a”、“b”或“c”编号).
(2)在同一时间内,表示不同反应的反应速率可以有:同温同压下放出氢气的体积V(H2);溶液中H+浓度的减少△c(H+);固体减少的量△m或△n.在0一t1s之间,设A1和Zn分别与盐酸反应的速率为v(Al)和v(Zn):
Ⅰ.若以溶液中c(H+)减少来表示不同反应的速率,即v(Al):v(Zn)═3:1;
Ⅱ.若以固体质量的减轻来表示不同反应的速率,即v(Al):v(Zn)═54:65;
Ⅲ.若以固体物质的量减少来表示不同反应的速率,即v(Al):v(Zn)═2:1.
IV.可以利用图2所示的装置测定不同浓度的硫酸与锌的反应速率,请回答下列问题:
按照上述装置图安装3套相同的装置,并检验装置气密性良好,将注射器的活栓推至“0”刻度处;然后在三个锥形瓶中分别放入相同形状的锌粒2g,并分别通过分液漏斗在锥形瓶中加入1mol•L-1、2mol•L-1和4mol•L-1的稀硫酸40mL.请补全下表空白:
| 序号 | 加入的稀硫酸浓度 | 反应时间/min | 收集的气体/mL | 反应速率mL•min-1 |
| ① | 1mol•L-1 | 11 | 10 | |
| ② | 2mol•L-1 | a | 10 | b |
| ③ | 4mol•L-1 | 10 | 5.0 |
A.12和0.83B.6和1.67C.1和10D.6和3.67.
 燃料电池是将乙醇通入负极,O2通入正极而发生电池反应的,其能量转换率高.
燃料电池是将乙醇通入负极,O2通入正极而发生电池反应的,其能量转换率高.