题目内容
2.为确定CH3CH2X分子中所含卤原子X的种类,可按下列步骤进行实验:a.取少量该卤代烃液体;b.加入适量NaOH溶液,加热;c.冷却后加入稀硝酸酸化;d.加入AgNO3溶液,观察反应现象.回答下列问题:
(1)①步骤b的目的是促进水解的进行;②步骤c的目的是中和NaOH.
(2)若加入AgNO3溶液时产生的沉淀为浅黄色,则此卤代烃中的卤素原子是Br(填元素符号).
(3)请写出步骤b中发生的化学反应的化学方程式(注明条件)CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr.
分析 (1)①卤代烃在碱性条件下完全水解;
②中和NaOH,使溶液呈酸性,有利于卤化银的沉淀;
(2)若生成的沉淀为淡黄色,则该沉淀为AgBr;
(3)CH3CH2Br在碱性条件下水解为乙醇和NaBr.
解答 解:(1)①卤代烃在碱性条件下完全水解,所以加入NaOH的目的是中和卤代烃水解产生的卤化氢,使水解完全,
故答案为:促进水解的进行;
②反应后的溶液中由剩余的NaOH,加入硝酸中和NaOH,使溶液呈酸性,有利于卤化银的沉淀,
故答案为:中和NaOH;
(2)若生成的沉淀为淡黄色,则该沉淀为AgBr,所以该卤代烃中的卤原子是Br,
故答案为:Br;
(3)CH3CH2Br在碱性条件下水解为乙醇和NaBr,故化学方程式为:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr,故答案为:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr.
点评 本题考查了卤代烃分子式的中卤素离子的检验方法,较基础,注意检验之前,先中和多余的碱,使溶液呈碱性.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
12.已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的四种溶液;
a.CH3COONa b.Na2CO3c.NaClO d.NaHCO3
pH由小到大排列的顺序是a<d<c<b(用编号填写).
(2)常温下,0.1mol•L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E.$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
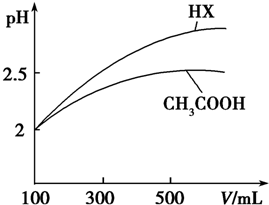
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是稀释相同倍数,一元酸HX的pH变化比CH3COOH的大,故HX酸性较强,电离平衡常数较大.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值).
(5)标准状况下,将1.12L CO2通入100mL 1mol•L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c (OH-)=2c(H2CO3)+c(HCO3-)+c(H+);②c(H+)+c(Na+)=c(HCO3-)+c(CO32-)+c(OH-).
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |

(1)物质的量浓度均为0.1mol•L-1的四种溶液;
a.CH3COONa b.Na2CO3c.NaClO d.NaHCO3
pH由小到大排列的顺序是a<d<c<b(用编号填写).
(2)常温下,0.1mol•L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E.$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是稀释相同倍数,一元酸HX的pH变化比CH3COOH的大,故HX酸性较强,电离平衡常数较大.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值).
(5)标准状况下,将1.12L CO2通入100mL 1mol•L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c (OH-)=2c(H2CO3)+c(HCO3-)+c(H+);②c(H+)+c(Na+)=c(HCO3-)+c(CO32-)+c(OH-).
13. 如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )
如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )
 如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )
如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )| A. | 变大 | B. | 变小 | C. | 不变 | D. | 无法判断 |
10.羟基是一种重要的官能团.某化学兴趣小组以①碳酸 ②苯酚 ③乙酸3种物质的溶液作为研究
对象,通过实验来比较不同物质的羟基中氢原子的活泼性.
某同学设计并实施了如下实验方案,请完成有关填空.
对象,通过实验来比较不同物质的羟基中氢原子的活泼性.
某同学设计并实施了如下实验方案,请完成有关填空.
| 编号 | 实验操作 | 实验现象 | 结论及解释 |
| 1 | 分别取3种溶液,滴加紫色石蕊溶液 | 溶液会变红的是①③ | |
| 2 | 用足量的乙酸溶液浸泡碳酸钙 | 有关反应的化学方程式为CaCO3+2CH3COOH=Ca(CH3COO)2+H2O+CO2↑ | |
| 3 | 将CO2通入苯酚钠溶液中 | 有关反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+NHCO3- | |
| 结论:3种物质的羟基中的氢原子的活泼性由强到弱的顺序是③①②(填序号) | |||
17.下列物质中属于氧化物的是( )
| A. | O2 | B. | Na2O | C. | NaClO | D. | FeSO |

 →
→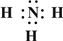 ,B的结构式为
,B的结构式为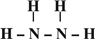 .
.