题目内容
6.下列物质能与SO2气体起反应,但无沉淀产生的是( )①溴水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3⑤稀H2SO4 ⑥Na2SO4 ⑦Na2SO3.
| A. | 只有① | B. | ①④⑤ | C. | ④⑥⑦ | D. | ①④⑦ |
分析 ①二氧化硫与溴水发生氧化还原反应生成硫酸和溴化氢;
②二氧化硫与氢氧化钡反应,二氧化硫少量反应生成亚硫酸钡沉淀,二氧化硫过量反应生成亚硫酸氢钡;
③二氧化硫与氢氧化钙反应,二氧化硫少量反应生成亚硫酸钙沉淀,二氧化硫过量反应生成亚硫酸氢钙;
④二氧化硫与碳酸钠反应生成亚硫酸钠和二氧化碳和水;
⑤二氧化硫与稀硫酸不反应;
⑥二氧化硫与硫酸钠不反应;
⑦二氧化硫与亚硫酸钠反应生成亚硫酸氢钠.
解答 解:①二氧化硫与溴水发生氧化还原反应生成硫酸和溴化氢,不会沉淀沉淀,故选;
②二氧化硫与氢氧化钡反应,二氧化硫少量反应生成亚硫酸钡沉淀,二氧化硫过量反应生成亚硫酸氢钡,二氧化硫少量产生沉淀,故不选;
③二氧化硫与氢氧化钙反应,二氧化硫少量反应生成亚硫酸钙沉淀,二氧化硫过量反应生成亚硫酸氢钙,二氧化硫少量产生沉淀,故不选;
④二氧化硫与碳酸钠反应生成亚硫酸钠和二氧化碳和水,不产生沉淀,故选;
⑤二氧化硫与稀硫酸不反应,故不选;
⑥二氧化硫与硫酸钠不反应,故不选;
⑦二氧化硫与亚硫酸钠反应生成亚硫酸氢钠,不会产生沉淀,故选;
故选:D.
点评 本题考查了元素化合物知识,熟悉二氧化硫的性质是解题关键,依据二氧化硫的酸性氧化物、还原性、氧化性的性质即可解答,题目难度不大.

练习册系列答案
相关题目
16.NA表示阿伏伽德罗常数,下列判断正确的是( )
| A. | 32gO2和O3混合气体中含有原子总数为NA | |
| B. | 含有NA个Na+的Na2O溶于1L水中,Na+的物质的量浓度为2mol/L | |
| C. | 标准状况下,22.4L空气含有NA个单质分子 | |
| D. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
17.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,22.4L庚烷完全燃烧所生成的气态产物的分子数为7 NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9 NA | |
| C. | 1mol乙烯分子中含有极性键数为4 NA | |
| D. | 1 mol醛基(-CHO)中含有的共用电子数为6 NA |
1.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去).下列推断正确的是( )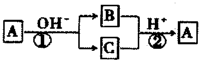

| A. | 反应①和②是可逆反应 | B. | 反应①和②一定为氧化还原反应 | ||
| C. | X元素可能是金属,也可能是非金属 | D. | X元素为铝 |
11.下列关于胶体的认识,正确的是( )
| A. | 是否能形成丁达尔效应是胶体和溶液最本质的区别 | |
| B. | 胶体具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 | |
| C. | 纳米材料粒子直径一般从几纳米到几十纳米(1 nm=10-9 m),因此纳米材料属于胶体 | |
| D. | 除去Fe(OH)3胶体中的FeCl3,可将混合物装入半透膜中,放入蒸馏水里 |
18.现有4.9gMgO、Mg(OH)2的固体混合物,与l00g9.8%的稀H2SO4恰好完全反应,形成不饱和溶液.则原固体混合物中镁元素的质量为( )
| A. | 1.2g | B. | 1.6g | C. | 2.4g | D. | 4.8g |
15.使用氢氧燃料电池的公共汽车已在北京街头出现.某种以30%KOH溶液为电解质的氢氧燃料电池在使用时的电极反应如下:
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能 | |
| D. | 氢氧燃料电池不属于环境友好电池 |
16.某烃的相对分子质量小于70,1mol该烃最多可与2mol H2发生加成反应,加成产物最多能与10mol Cl2发生取代反应,则该烃的分子式为( )
| A. | C3H6 | B. | C3H4 | C. | C4H6 | D. | C5 H8 |