题目内容
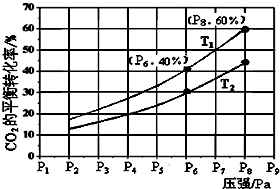
18. (1)汽车尾气是造成空气污染产生雾霾的原因之一.其中涉及的反应2NO(g)+O2?2NO2(g)在其他条件不变达平衡时.分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线如图所示.
(1)汽车尾气是造成空气污染产生雾霾的原因之一.其中涉及的反应2NO(g)+O2?2NO2(g)在其他条件不变达平衡时.分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线如图所示.①比较P1、P2的大小关系:p1<p2.
②当温度升高时,该反应平衡常数变化的趋势是减小.
(2)研究氮氧化物与悬浮在大气中海盐离子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g) K1△H<0 (Ⅰ)
2NO(g)+Cl2(g)?2ClNO(g) K2△H<0 (Ⅱ)
①4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=$\frac{{K}_{1}^{2}}{{K}_{2}}$(用K1、K2表示).
②为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应(Ⅱ)达到平衡.测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=0.025 mol,NO的转化率а1=75%.其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率а2>а1(填“>”“<”或“=”),平衡常数K2不变(填“增大”“减小”或“不变”.若要使K2减小,可采用的措施是升高温度.
分析 (1)①已知2NO(g)+O2(g)?2N02(g)是正方向体积减小的反应,根据压强对平衡的影响分析;
②根据图象2判断该反应正方向是放热还是吸热,再判断K随温度的变化;
(2)已知:①2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g),
②2NO(g)+Cl2(g)?2ClNO(g),
根据盖斯定律①×2-②可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数为①的平衡常数平方与②的商;
②测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,由方程式计算参加反应NO、氯气的物质的量,进而计算平衡时氯气的物质的量、NO的转化率;
正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,反应(Ⅱ)在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动;
平衡常数只受温度影响,温度不变,平衡常数不变.
解答 解:(1)①已知2NO(g)+O2(g)?2N02(g)是正方向体积减小的反应,增大压强平衡正移,则NO的转化率会增大,由图可知p2时NO的转化率大,则p2时压强大,即p1<p2;故答案为:p1<p2;
②由图象2可知,随着温度的升高,NO的转化率减小,说明升高温度平衡逆移,则该反应正方向是放热反应,所以升高温度平衡常数K减小;故答案为:减小;
(2)2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g) K1 △H<0 (I)
2NO(g)+Cl2(g)?2ClNO(g) K2 △H<0 (II)
根据盖斯定律,Ⅰ×2-Ⅱ可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数K=$\frac{{K}_{1}^{2}}{{K}_{2}}$,故答案为:$\frac{{K}_{1}^{2}}{{K}_{2}}$;
②测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,
由方程式可知,参加反应氯气的物质的量为0.15mol×$\frac{1}{2}$=0.075mol,故平衡时氯气的物质的量为0.1mol-0.075mol=0.025mol;
参加反应NO物质的量为0.15mol,则NO的转化率为$\frac{0.15mol}{0.2mol}$×100%=75%;
正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,反应(Ⅱ)在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动,NO转化率增大,故转化率α2>α1;
平衡常数只受温度影响,温度不变,平衡常数不变,即平衡常数K2 不变,正反应是放热反应可以升高温度使K2减小,
故答案为:0.025;75%;>;不变;升高温度.
点评 本题考查化学平衡计算与影响因素、化学平衡常数等,侧重考查学生分析计算能力,需要学生具备扎实的基础与灵活应用能力,难度中等.

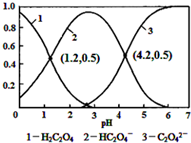
| A. | pH=1.2溶液中:c(K+)+c(H+)═c(OH-)+c(H2C2O4) | |
| B. | pH=2.7溶液中:$\frac{{c}^{2}(H{C}_{2}{O}_{4}^{-})}{c({H}_{2}{C}_{2}{O}_{4})}$×c(C2O42-)=1000 | |
| C. | 将相同物质的量KHC2O4和K2C2O4固体完全溶于水所得混合液的pH为4.2 | |
| D. | 向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度一定增大 |
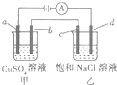 如图所示,a,b,c均为石墨电极,d为碳钢电极,通电电解一段时间,假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a,b,c均为石墨电极,d为碳钢电极,通电电解一段时间,假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A. | 甲、乙两烧杯中溶液的pH均保持不变 | |
| B. | 甲烧杯中b电极反应式为:Cu2++2e-═Cu | |
| C. | 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 | |
| D. | 当b极增重3.2g时,d极产生的气体为0.56L(标准状况) |
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④⑤ |
| A. | 金刚石 | B. | 砖瓦 | C. | 水晶 | D. | 大理石 |

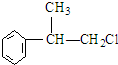 ,
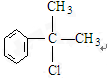
,
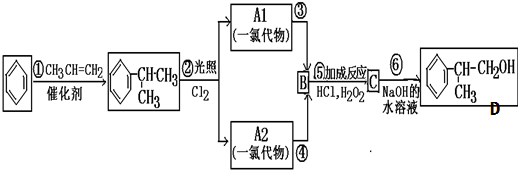
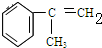 C的结构简式:
C的结构简式: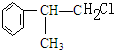 .
.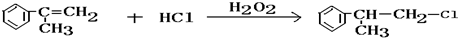 .
.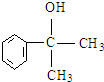 等.
等.