题目内容
7.工业上使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如图1: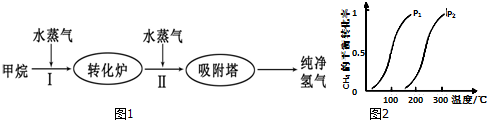
(1)此流程的第I步反应为:CH4(g)+H2O(g)?CO(g)+3H2(g),
一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1<P2(填“<”、“>”或“=”).
100℃时,将1mol CH4和2mol H2O通入容积为100L的恒容密闭容器中,达到平衡时CH4的转化率为0.5.此时该反应的平衡常数K=2.25×10-4.
(2)此流程的第II步反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
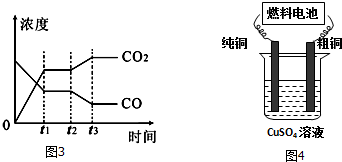
图3表示该反应在t1时刻达到平衡,在t2时刻因改变某个条件引起浓度变化的情况,图中t2时刻发生改变的条件是降低温度,或增加水蒸汽的量,或减少氢气的量(写出一种).
(3)工业上常利用第Ⅰ步反应产生的CO和H2在“催化反应室”中合成二甲醚(CH3OCH3).在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
催化反应室中总反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的△H=-246.1kJ/mol.
(4)用二甲醚-空气碱性(KOH)燃料电池作电源电解精炼粗铜(见图4),在接通电路一段时间纯铜质量增加6.4g.
请写出燃料电池中的正极反应式:O2+2H2O+4e-=4OH-.
燃料电池正极消耗空气的体积是5.6L(标准状况,空气中O2体积分数以20%计算).
分析 (1)采取控制变量法分析,由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动;依据化学平衡三段式列式计算平衡浓度结合平衡常数概念计算得到,平衡常数随温度变化;
(2)分析图表数据可知平衡常数随温度升高减小,说明平衡逆向进行,正反应是放热反应;在t2时刻因改变某个条件浓度发生变化的情况是二氧化碳浓度增大,一氧化碳浓度减小,结合平衡移动原理分析;
(3)根据盖斯定律结合已知反应来书写热化学方程式,加减法求焓变;
(4)燃料电池中,负极上是燃料发生失电子的氧化反应,正极是氧气发生得电子的还原反应,根据氧气和空气之间的组成关系来回答.
解答 解:(1)由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,平衡向正反应方向移动,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动,即P1<P2;100℃时,将1mol CH4和2mol H2O通入容积为100L的恒容密闭容器中,达到平衡时CH4的转化率为0.5,
CH4(g)+H2O(g)?CO(g)+3H2(g)
起始量(mol/L) 0.01 0.02 0 0
变化量(mol/L) 0.005 0.005 0.005 0.015
平衡量(mol/L) 0.005 0.015 0.005 0.015
平衡常数K=$\frac{c(CO)c{\;}^{3}(H{\;}_{2})}{c(CH{\;}_{4})c(H{\;}_{2}O)}$=$\frac{0.005×(0.015){\;}^{3}}{0.005×0.015}$=2.25×10-4(mol/L)2,
故答案为:<;2.25×10-4;
(2)分析图表数据可知平衡常数随温度升高减小,说明平衡逆向进行,正反应是放热反应;CO(g)+H2O(g)?H2(g)+CO2(g),反应是气体体积不变的放热反应,在t2时刻因改变某个条件浓度发生变化的情况是二氧化碳浓度增大,一氧化碳浓度减小,说明平衡正向进行,降低温度,或增加水蒸气的量或减少氢气的量均可以实现,
故答案为:放热;降低温度,或增加水蒸汽的量,或减少氢气的量;
(3)已知:①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol,
反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)可以根据①×2+③+②得到,得出此反应的△H=-246.1kJ/mol,
故答案为:-246.1kJ/mol;
(4))燃料电池中,负极上是燃料甲醚发生失电子的氧化反应,在碱性环境下,发生的反应为:CH3OCH3-12e-+16OH-=2CO32-+11H2O,燃料电池正极上发生的电极反应为:O2+2H2O+4e-=4OH-,纯Cu是阴极,该极上析出金属铜,当质量增加6.4g,转移电子为0.2mol,此时正极上消耗氧气的物质的量是0.05mol,所以需要空气的体积是0.05mol×5×22.4L/mol=5.6L,
故答案为:O2+2H2O+4e-=4OH-;5.6.
点评 本题考查了化学平衡的分析判断,图象分析方法,平衡常数的计算应用,平衡移动原理的理解和影响因素的分析是解题关键,题目难度适中.

 阅读快车系列答案
阅读快车系列答案| A. | Na2CO3 | B. | Na2O2 Na2CO3 | ||
| C. | NaOH Na2CO3 | D. | Na2O2 NaOH Na2CO3 |
| A. | 为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气 | |
| B. | 酸雨的PH小于5.6 | |
| C. | SO2可以用作食物和干果的防腐剂 | |
| D. | 铵盐受热易分解,都生成氨气和对应的酸 |
| A. | 含非极性键的分子一定是非极性分子 | |
| B. | 含有极性键的分子一定是极性分子 | |
| C. | 非极性分子一定含有非极性键 | |
| D. | 极性分子不一定只含有极性键 |
| 物质 | A | B | C | D |
| 反应前质量(g) | 4 | 6 | 111 | 4 |
| 反应后质量(g) | 待测 | 15 | 0 | 84 |
| A. | 该反应的反应物为A和C | |
| B. | 容器中发生的化学反应,属于分解反应 | |
| C. | 反应后,生成了84g D物质 | |
| D. | 反应后,待测A的质量为26 g |
| A. | KCl | B. | MgO | C. | K2S | D. | NaF |

| A. | 用装置甲在光照条件下验证甲烷与氯气的反应 | |
| B. | 用装置乙除去甲烷中少量的乙烯得纯净甲烷 | |
| C. | 装置丙用于实验室制取NH3 | |
| D. | 用装置丁分馏石油并收集60~150℃馏分 |
 .
.