题目内容
13.下列物质中存在离子键和非极性键的是( )| A. | NaOH | B. | NH4Cl | C. | CaC2 | D. | H2O2 |
分析 活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,据此分析解答.
解答 解:A.NaOH中钠离子和氢氧根离子之间存在离子键、O-H原子之间存在极性键,故A错误;
B.NH4Cl中铵根离子和氯离子之间只存在离子键,N与H原子之间为极性键,故C错误;
C.碳化钙中钙离子和C22-离子之间存在离子键、C-C原子之间存在非极性键,故C正确;
D.双氧水分子中O-H之间存在极性键、O-O之间存在非极性键,故D错误;
故选C.
点评 本题考查离子键、非极性键判断,侧重考查基本概念,明确离子键、共价键概念内涵及其区别是解本题关键,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
1.公共场所常使用一种电离式烟雾报警器,其主体是一个放有镅-241(${\;}_{95}^{241}$Am)放射源的电离室.${\;}_{95}^{241}$Am含有的中子数是( )
| A. | 51 | B. | 95 | C. | 146 | D. | 241 |
8.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯化铁溶液溶解铜 Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OH-═SO42-+H2O |
5.下列各组中两种溶液间的反应,均可用同一离子方程式表示的是( )
| A. | CH3COOH和Na2CO3与CH3COOH和NaHCO3 | |
| B. | AgNO3和HCl与AgNO3和NaCl | |
| C. | BaCl2和Na2SO4 与Ba(OH)2和H2SO4 | |
| D. | KOH和AlCl3与氨水和AlBr3 |

 可以循环利用的副产物是 。
可以循环利用的副产物是 。 如图所示装置:
如图所示装置: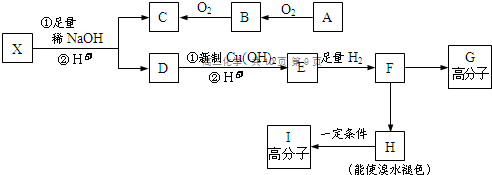
 →CH3-CHO+H2O
→CH3-CHO+H2O ;
; ;
; ;
;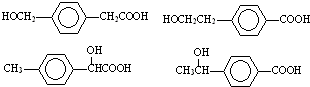 任意一种.
任意一种.