题目内容
2.按要求书写下列反应的离子方程式(1)84消毒液(NaClO)和浓盐酸不能混用ClO-+Cl-+2H+=Cl2↑+H2O
(2)向碘水中滴加NaSO3溶液I2被还原为I-的反应SO32-+I2+H2O=2I-+SO42-+2H+
(3)足量Ca(OH)2溶液与NaHCO3溶液反应Ca2++HCO3-+OH-=CaCO3↓+H2O
(4)漂白粉的制备反应2Ca(OH)2+2Cl2=2Ca2++2Cl-+2ClO-+2H2O
(5)少量的氯气和溴化亚铁反应Cl2+2Fe2+=2Cl-+2Fe3+.
分析 (1)次氯酸根离子与盐酸反应生成氯气和水;
(2)碘单质与亚硫酸根离子发生氧化还原反应生成硫酸根离子和碘离子、氢离子;
(3)氢氧化钙足量反应生成碳酸钙、氢氧化钠和水;
(4)氯气通入石灰乳生成氯化钙、次氯酸钙和水;
(5)氯气少量,只氧化二价铁离子.
解答 解:(1)次氯酸根离子与氯离子在酸性环境下反应生成氯气和水,离子方程式:ClO-+Cl-+2H+=Cl2↑+H2O;
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
(2)碘单质与亚硫酸根离子发生氧化还原反应生成硫酸根离子和碘离子、氢离子,离子方程式:SO32-+I2+H2O=2I-+SO42-+2H+;
故答案为:SO32-+I2+H2O=2I-+SO42-+2H+;
(3)足量Ca(OH)2溶液与NaHCO3溶液反应,离子方程式:Ca2++HCO3-+OH-=CaCO3↓+H2O;
故答案为:Ca2++HCO3-+OH-=CaCO3↓+H2O;
(4)氯气通入石灰乳生成氯化钙、次氯酸钙和水,离子方程式:2Ca(OH)2+2Cl2=2Ca2++2Cl-+2ClO-+2H2O;
故答案为:2Ca(OH)2+2Cl2=2Ca2++2Cl-+2ClO-+2H2O;
(5)少量的氯气和溴化亚铁反应,反应离子方程式:Cl2+2Fe2+=2Cl-+2Fe3+,
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
12.下列有机物的命名正确的一项是( )
| A. | (CH3)2CHCH(CH3)2:2-二甲基丁烷 | B. | CH3CH(OH)CH(CH3)2:3-甲基-2-丁醇 | ||
| C. |  :1,4-二甲苯 :1,4-二甲苯 | D. |  :正丁酸甲酯 :正丁酸甲酯 |
13.下列物质中存在离子键和非极性键的是( )
| A. | NaOH | B. | NH4Cl | C. | CaC2 | D. | H2O2 |
7.在密闭容器中充入N2和H2,合成NH3,到2秒末测得,v (H2)═0.45mol/(L•s),则2秒末NH3的浓度为( )
| A. | 0.5 mol/L | B. | 0.45 mol/L | C. | 0.6 mol/L | D. | 0.55 mol/L |
14.下列说法正确的是( )
| A. | 取少许某溶液,滴加数滴KSCN溶液,无明显现象;再另取少许原溶液,先滴少量新制氯水,再滴加数滴KSCN溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| B. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色,然后蘸取溶液 | |
| C. | 在淀粉溶液中加入稀硫酸并加热片刻后,再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 | |
| D. | 测定某溶液的pH,常用干燥洁净的玻璃棒蘸取该溶液滴在润湿的pH试纸上 |
11.下列物理量中不是国际单位制的七个基本物理量之一的是( )
| A. | 物质的量 | B. | 密度 | C. | 长度 | D. | 质量 |
12.用铁片与稀硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是( )
| A. | 加热 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 加入硫酸铜 | D. | 不用铁片,改用铁粉 |
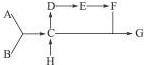 A、B、C、D、E、F、G、H八种物质间存在着如下图所示的变化关系,其中A、B为单质,相对分子质量A大于B;E在通常状况下为有颜色,有刺激性气味的气体;H为一种氯化物,与碱石灰共热可制取C;G中含A元素35%.
A、B、C、D、E、F、G、H八种物质间存在着如下图所示的变化关系,其中A、B为单质,相对分子质量A大于B;E在通常状况下为有颜色,有刺激性气味的气体;H为一种氯化物,与碱石灰共热可制取C;G中含A元素35%. .
. .
.