题目内容
5.乙酸的下列性质中,可以证明它是弱电解质的是( )| A. | 乙酸与水能以任意比例互溶 | |
| B. | 乙酸溶液的导电性弱 | |
| C. | 10 mL1 mol•L-1乙酸恰好与10 mL1 mol•L-1NaOH溶液完全反应 | |
| D. | 1 mol•L-1的乙酸溶液的C(H+)约为0.01 mol•L-1 |
分析 A.乙酸与水以任意比例互溶,这是乙酸的物理性质,不能证明是弱电解质;
B.溶液的导电性取决于自由移动离子浓度和自由移动离子带电数目;
C.是中和反应,按照反应方程式进行;
D.乙酸是弱电解质,不能完全电离.
解答 解:A.乙酸水溶性是物理性质,不能证明是弱电解质,故A错误;
B.缺少条件,溶液浓度不确定,乙酸溶液的导电性比盐酸溶液可能强也可能弱,故B错误;
C.根据方程式可知不论酸碱强弱,只有一元酸与一元碱物质的量相等则恰好发生酸碱中和,完全反应,故C错误;
D.1mol•L-1的乙酸溶液的c(H+)约为0.01mol•L-1说明乙酸不能完全电离,可以证明是弱电解质,故D正确;
故选D.
点评 本题考查了弱电解质的判断,题目难度不大,注意把握住弱电解质的定义“部分电离”的特点.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
15.下列说法正确的是( )
| A. | 阴离子只有还原性 | |
| B. | 含有最高价元素的化合物,只有氧化性,不具有还原性 | |
| C. | Zn和稀硫酸反应既属于离子反应,也属于氧化还原反应 | |
| D. | 没有单质参加也没有单质生成的反应一定不是氧化还原反应 |
20.下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )
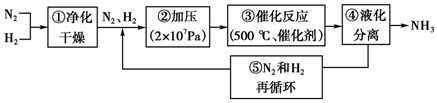

| A. | ①②③ | B. | ①③⑤ | C. | ②④ | D. | ②③④ |
17.Se是人体必需的微量元素,下列有关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的说法正确的是( )
| A. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的核外电子数不同 | |
| B. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的中子数分别为78和80 | |
| C. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质量数不同,是同种元素 | |
| D. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质子数相同,是同一种核素 |
14.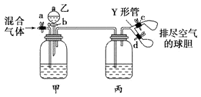 用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )
用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )
 用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )
用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )| 甲 | 乙 | 丙 | |
| A | 饱和NaHCO3溶液 | 12mol•L-1盐酸 | 18.4mol•L-1 H2SO4 |
| B | 饱和Na2CO3溶液 | 2mol•L-1 H2SO4 | 饱和NaOH溶液 |
| C | 饱和NaOH溶液 | 2mol•L-1 H2SO4 | 18.4mol•L-1 H2SO4 |
| D | 18.4mol•L-1 H2SO4 | 饱和NaOH溶液 | 18.4mol•L-1 H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
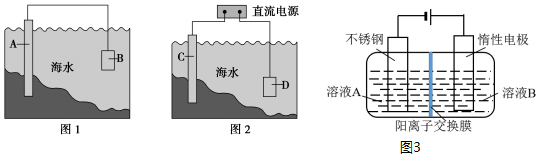
 “套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题:
“套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题: 某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: