题目内容
3.SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:①SO2+2Fe3++2H2O═SO42-+2Fe2++4H+②Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O下列有关说法不正确的是( )
| A. | SO2发生氧化反应 | |
| B. | 氧化性:Cr2O72->Fe3+>SO42- | |
| C. | 每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA | |
| D. | 若6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7 |
分析 SO2+2Fe3++2H2O═SO42-+2Fe2++4H+中,S元素的化合价升高,Fe元素的化合价降低;
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O中,Cr元素的化合价降低,Fe元素的化合价升高,结合氧化还原反应基本概念来解答.
解答 解:SO2+2Fe3++2H2O═SO42-+2Fe2++4H+中,S元素的化合价升高,Fe元素的化合价降低;
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O中,Cr元素的化合价降低,Fe元素的化合价升高,
A.S失去电子被氧化,可知SO2发生氧化反应,故A正确;
B.由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性为Cr2O72->Fe3+>SO2,故B正确;
C.每有1 mol K2Cr2O7参加反应,转移电子为1mol×2×(6-3)=6mol,转移电子的数目为6NA,故C正确;
D.若6.72 L SO2(标准状况)参加反应,n(SO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,由电子守恒可知,消耗K2Cr2O7为$\frac{0.3mol×(6-4)}{2×(6-3)}$=0.1mol,故D错误;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意氧化性比较及电子守恒的应用,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
8.下列物质中一氯代物有4种的是:( )
| A. | 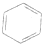 | B. | 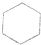 | C. | 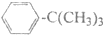 | D. | CH3CH2CH(CH2CH3)2 |
11.一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为55.2g,若其中水的质量为21.6g,则CO的质量为( )
| A. | 2.8g | B. | 4.4g | C. | 8.8g | D. | 4.4~8.8g |
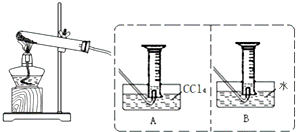
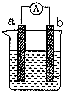 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: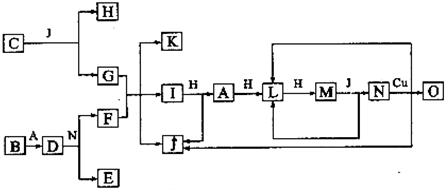
 .
.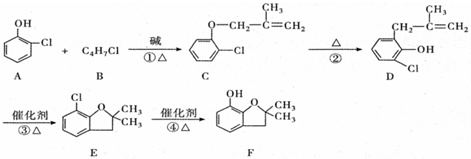
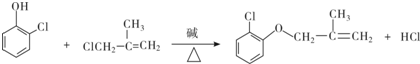 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).