题目内容
11.一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为55.2g,若其中水的质量为21.6g,则CO的质量为( )| A. | 2.8g | B. | 4.4g | C. | 8.8g | D. | 4.4~8.8g |
分析 由一定质量的乙醇燃烧得到H2O的质量为21.6g,根据n=$\frac{m}{M}$计算水的物质的量,根据N原子守恒计算乙醇物质的量,根据原子守恒计算CO、CO2的总的物质的量,结合二者质量之和列方程计算各自物质的量,根据m=nM计算CO的质量.
解答 解:n(H2O)=$\frac{21.6g}{18g/mol}$=1.2mol,
根据H原子守恒,可知乙醇的物质的量=$\frac{1.2mol×2}{6}$=0.4mol,
根据C原子守恒,可知CO和CO2的总的物质的量=0.4mol×2=0.8mol,
由于水的质量为21.6g,所以一氧化碳和二氧化碳的质量为:55.2g-21.6g=33.6g;
令CO、CO2的物质的量分别为xmol、ymol,则:
$\left\{\begin{array}{l}{x+y=0.8}\\{28x+44y=33.6}\end{array}\right.$
解得x=0.1,y=0.7,
所以原混合气中CO的质量为0.1mol×28g/mol=2.8g,
故选:A.
点评 本题考查混合物的有关计算,难度中等,关键是抓住化学反应前后原子守恒守恒及质量守恒解答.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
15.下列说法不正确的是( )
| A. | 仅含碳、氢元素的有机物称为烃 | |
| B. | 1,2-二溴乙烷是无色液体 | |
| C. | 溴苯的密度比水大 | |
| D. | 四氟乙烯(CF2=CF2)中含有碳碳双键,属于烯烃 |
16.常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )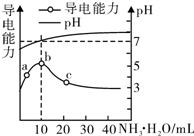

| A. | HR为强酸 | |
| B. | b点溶液呈中性,说明NH4R没有水解 | |
| C. | c点溶液存在c(NH4+)<c( R-) | |
| D. | b~c任意点溶液均有c(H+)×c(OH-)=l.0×l0-14 |
16.一定条件下:甲分子和乙反应应生成丙分子和丁分子,下列不正确的是( )


| A. | 该反应类型是置换反应 | B. | 甲的空间构型是平面正六边形 | ||
| C. | 丙不属于烃类物质 | D. | 分离甲和丙可以采用蒸馏法 |
3.SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:①SO2+2Fe3++2H2O═SO42-+2Fe2++4H+②Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
下列有关说法不正确的是( )
下列有关说法不正确的是( )
| A. | SO2发生氧化反应 | |
| B. | 氧化性:Cr2O72->Fe3+>SO42- | |
| C. | 每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA | |
| D. | 若6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7 |
20.两种金属的混合物3g投入水中,收集到1.12L氢气(标准状况),不可能构成此种混合物的是( )
| A. | Li和Na | B. | Rb和Ca | C. | Na和Cu | D. | K和Na |
1.用光洁的铂丝蘸取某无色溶液,在无色灯焰中灼烧时,观察到黄色火焰,下列有关叙述中正确的是( )
| A. | 只有Na+ | B. | 可能含Na+,也可能含K+ | ||
| C. | 既有Na+又有K+ | D. | 一定含Na+,也可能含K+ |
