题目内容
对同温同压下的两种气体12C18O和14N2的有关比较正确的是( )
| A、质量相等时所含质子数相等 |
| B、体积不相等时密度有可能相等 |
| C、体积相等时所含电子数相等 |
| D、原子数相等时所含中子数相等 |
考点:核素,质量数与质子数、中子数之间的相互关系
专题:
分析:同温同压下,气体的Vm相等,等体积时,根据n=
可知气体的物质的量相等,结合原子的构成以及相关物理量的计算公式解答该题.
| V |
| Vm |
解答:
解:A、12C18O和14N2分子内均有14个质子,由于二者的相对分子质量不等,故等质量的两种分子所具有的质子数不等,故A错误;
B、由于12C18O和14N2的相对分子质量不等,故体积相等的两种气体的质量不等,因此密度不等,故B错误;
C、12C18O和14N2均为14电子分子,同温同压下,体积相等则分子数相等,所具有的电子数相等,故C正确;
D、1个12C18O分子中有16个中子,1个14N2分子中含有14个中子,二者均为双原子分子,原子数相等,即分子数相等,但中子数不等,故D错误,
故选C.
B、由于12C18O和14N2的相对分子质量不等,故体积相等的两种气体的质量不等,因此密度不等,故B错误;
C、12C18O和14N2均为14电子分子,同温同压下,体积相等则分子数相等,所具有的电子数相等,故C正确;
D、1个12C18O分子中有16个中子,1个14N2分子中含有14个中子,二者均为双原子分子,原子数相等,即分子数相等,但中子数不等,故D错误,
故选C.
点评:本题考查基本概念和基本理论知识,意在考查考生对一些重要概念与理论的理解能力,题目难度中等.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
下表是3种物质的溶解度(20℃),下列说法中正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.000 84 | 0.01 |
| A、已知MgCO3的Ksp=6.82×10-6 mol2?L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2?L-2 |
| B、除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液 |
| C、将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 |
| D、用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+MgCO3↓+2H2O |
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、Z的说法正确的是( )


| A、相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B、Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
| C、ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D、由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA |
| B、标况下,22.4L NO与11.2L O2混合后气体的分子数为2NA |
| C、标准状况下,22.4 L己烷中共价键数目为19NA |
| D、常温常压下,将0.1mol Fe投入足量的浓硝酸中,转移的电子数为0.3 NA |
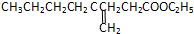
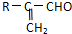
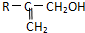
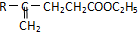
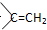 ,核磁共振氢谱有3个峰,且峰面积之比为9:2:1的同分异构体的结构简式为
,核磁共振氢谱有3个峰,且峰面积之比为9:2:1的同分异构体的结构简式为