题目内容
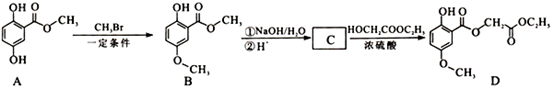
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、Z的说法正确的是( )


| A、相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B、Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
| C、ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D、由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:这几种元素都是短周期元素,根据元素在周期表中的位置知,X是He、Y是F、Z是S元素,
A.元素的非金属性越强,其单质与氢气反应越剧烈;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.二氧化硫和硫酸不反应;
D.H、O、S元素形成的常见化合物有硫酸、亚硫酸,非金属元素之间易形成共价键.
A.元素的非金属性越强,其单质与氢气反应越剧烈;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.二氧化硫和硫酸不反应;
D.H、O、S元素形成的常见化合物有硫酸、亚硫酸,非金属元素之间易形成共价键.
解答:
解:这几种元素都是短周期元素,根据元素在周期表中的位置知,X是He、Y是F、Z是S元素,
A.元素的非金属性越强,其单质与氢气反应越剧烈,X原子最外层达到稳定结构,性质较不活泼,和氢气不易反应,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性F>S,所以Y的气态氢化物稳定性比Z的气态氢化物的稳定性强,故B正确;
C.Z的最高价氧化物的水化物是硫酸,浓硫酸具有强氧化性,但不能氧化二氧化硫,故C错误;
D.H、O、S元素形成的常见化合物有硫酸、亚硫酸,非金属元素之间易形成共价键,所以硫酸、亚硫酸中只含共价键,故D错误;
故选B.
A.元素的非金属性越强,其单质与氢气反应越剧烈,X原子最外层达到稳定结构,性质较不活泼,和氢气不易反应,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性F>S,所以Y的气态氢化物稳定性比Z的气态氢化物的稳定性强,故B正确;
C.Z的最高价氧化物的水化物是硫酸,浓硫酸具有强氧化性,但不能氧化二氧化硫,故C错误;
D.H、O、S元素形成的常见化合物有硫酸、亚硫酸,非金属元素之间易形成共价键,所以硫酸、亚硫酸中只含共价键,故D错误;
故选B.
点评:本题考查元素周期表和元素周期律的综合应用,侧重考查分析、推断能力,熟练掌握元素周期律、物质结构,注意浓硫酸不能氧化二氧化硫但能氧化硫化氢,易错选项是C.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )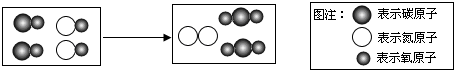

| A、图中单质的化学式为N2 |
| B、该反应使有毒气体转化为无毒气体 |
| C、反应物都属于氧化物 |
| D、反应中原子、分子个数都不变 |
下列说法中正确的是( )
| A、在酸性环境中钢铁发生析氢腐蚀 |
| B、电解质溶液为氢氧化钠溶液,铝和镁形成原电池时,镁作负极 |
| C、铅蓄电池中铅做正极,PbO2做负极,两极浸在H2SO4溶液中 |
| D、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 |
设NA代表阿伏加德罗常数的数值,则下列说法正确的是( )
| A、1.8 g D2O含有NA个中子 |
| B、用5 mL 3 mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
| C、在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4 L的CO2 |
| D、25℃时,7 g C2H4和C3H6的混合气体中,含有NA个C-H键 |
对同温同压下的两种气体12C18O和14N2的有关比较正确的是( )
| A、质量相等时所含质子数相等 |
| B、体积不相等时密度有可能相等 |
| C、体积相等时所含电子数相等 |
| D、原子数相等时所含中子数相等 |
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++OH-=H2O | ||||
B、氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH-
| ||||
| C、氢氧化镁与稀硫酸反应:H++OH-═H2O | ||||
| D、单质铜与稀硝酸反应:Cu+2H++2NO3-═Cu2++2NO↑+H2O |