题目内容
某密闭容器中有如下可逆反应:A(气)+2B(气)═2C(气)△H<0,达到平衡后,若改变反应条件将变化的情况填入空格:
(1)升高温度,v(正) ,v(逆) (填增大、减小、不变)、平衡向 移动
(2)加入催化剂,A的物质的量 ,v(正) ,v(逆) (填增大、减小、不变)、平衡 移动.
(3)缩小容器的体积,则C的物质的量 ,A的转化率 (填增大、减小、不变)、平衡向 移动.
(1)升高温度,v(正)
(2)加入催化剂,A的物质的量
(3)缩小容器的体积,则C的物质的量
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)反应是放热反应,升温化学反应速率增大,平衡向吸热反应方向进行;
(2)加入催化剂改变反应速率,不改变化学平衡;
(3)缩小容器体积增大压强平衡正向进行;
(2)加入催化剂改变反应速率,不改变化学平衡;
(3)缩小容器体积增大压强平衡正向进行;
解答:
解:可逆反应:A(气)+2B(气)═2C(气)△H<0,反应是气体体积减小的放热反应
(1)反应是放热反应,升温化学反应速率增大,正逆反应速率都增大,平衡向吸热反应方向进行,平衡逆向进行;
故答案为:增大,增大,逆向;
(2)加入催化剂改变反应速率,同等程度增大正逆反应速率,但不改变化学平衡,A的物质的量不变;
故答案为:不变,增大,增大,不;
(3)缩小容器体积增大压强平衡正向进行,C的物质的量增大,A的转化率增大;
故答案为:增大,增大,正向;
(1)反应是放热反应,升温化学反应速率增大,正逆反应速率都增大,平衡向吸热反应方向进行,平衡逆向进行;
故答案为:增大,增大,逆向;
(2)加入催化剂改变反应速率,同等程度增大正逆反应速率,但不改变化学平衡,A的物质的量不变;
故答案为:不变,增大,增大,不;
(3)缩小容器体积增大压强平衡正向进行,C的物质的量增大,A的转化率增大;
故答案为:增大,增大,正向;
点评:本题考查了化学平衡移动原理的分析判断,注意反应特征和移动原理的分析应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列关于有机物说法正确的是( )
| A、制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中 |
| B、纤维素和淀粉都是多糖,二者互为同分异构体 |
| C、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| D、三大合成材料是塑料、合成纤维和合成橡胶 |
海藻中含有丰富的、以各种无机盐形式存在的碘元素,下图是实验室从海藻里提取碘的流程的一部分.下列判断正确的是( )


| A、步骤①、③、④的操作分别是过滤、萃取、分液 |
| B、可用淀粉溶液检验步骤②的反应是否进行完全 |
| C、步骤③中加入的有机溶剂是汽油或酒精 |
| D、步骤②之后的碘均为游离态 |
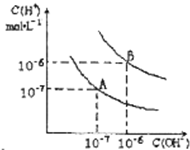 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: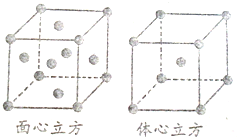 (1)氯化铝常温下为固体,熔点190℃(253kPa),易升华.实验室氯化铝蒸气的密度为11.92g?L-1(已折算成标准状况),据此判断氯化铝晶体为
(1)氯化铝常温下为固体,熔点190℃(253kPa),易升华.实验室氯化铝蒸气的密度为11.92g?L-1(已折算成标准状况),据此判断氯化铝晶体为