题目内容
7.下列粒子属于等电子体的是( )| A. | CH4和NH3 | B. | N2和CO | C. | NH2-和H3O+ | D. | HCl和H2O |
分析 等电子体有两个相等,一是价电子数相等,二是原子数目相等.
解答 解:A.CH4和NH3,原子数不同,不是等电子体,故A错误;
B.N2和CO原子数相等,价电子数分别是5×2=10、4+6=10,是等电子体,故B正确;
C.NH2-和H3O+,原子数不同,不属于等电子体,故C错误;
D.HCl和H2O,原子数不同,不是等电子体,故D错误;
故选:B.
点评 本题考查了等电子体的含义,解答本题的关键是要充分理解等电子体的本质特征,只有这样才能对问题做出正确的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.X是某元素的一种同位素,该原子的质量数为A,中子数为N,它的气态氢化物为XH3,则它与18O形成的最高价气态氧化物ag中含有质子的物质的量为( )
| A. | $\frac{a(A-N+3)}{A+3}$mol | B. | $\frac{a(A-N+8)}{A+16}$mol | ||
| C. | $\frac{a(2A-2N+40)}{2A+90}$mol | D. | $\frac{2A-2N+24}{2A+54}$mol |
2.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C-C≡C-C≡C-C≡C-C≡N.对该物质判断正确的是( )
| A. | 该物质与乙炔互为同系物 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 不能发生加聚反应 | |
| D. | 可由乙炔和含氮化合物通过取代反应制得 |
19.某一元醛发生银镜反应可得21.6g银,将等量的醛完全燃烧,生成3.6g H2O,此醛可能是( )
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 戊醛 |
16.能充分说明可逆反应N2(g)+O2(g)?2NO(g)已达到平衡状态的是( )
| A. | O2的消耗速率等于NO的消耗速率 | |
| B. | 容器内始终有N2、O2和NO共存 | |
| C. | 容器内反应混合物的总物质的量不随时间改变 | |
| D. | V正(N2)=V逆(N2) |
17.下列排列顺序正确的是( )
| A. | 还原性:F->Cl->Br->I- | |
| B. | 酸性:碳酸>石碳酸>碳酸氢钠>氢氧化铝 | |
| C. | 氧化性:Na>S>F2>O2 | |
| D. | NaHCO3溶液:c(HCO3-)>c(CO32-)>c(OH-) |
 已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答:
已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答: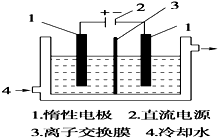 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.