题目内容
15.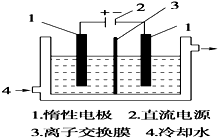 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
(1)碘是紫黑色物质,实验室常用升华方法来分离提纯含有少量杂质的固体碘.
(2)写出碘酸钾在酸性介质中与过氧化氢反应的离子方程式:2IO3-+2H++5H2O2=I2↓+5O2↑+6H2O
(3)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.图中的序号3应为阴离子交换膜(填“阳”或“阴”);电解时,阳极上发生反应的电极反应式为I-+6OH--6e-=IO3-+3H2O.
(4)教材中利用KI与空气的反应来探究反应速率与温度的关系,现有1mol/L的KI溶液、0.1mol/L的H2SO4溶液、淀粉溶液,则实验时这几种试剂的加入顺序为:
KI溶液、淀粉溶液、0.1mol/LH2SO4溶液;反应的离子方程式为4H++4I-+O2=2I2+2H2O.
(5)已知KI+I2?KI3,将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?否(填“是”或“否”),并说明理由低温制备的KI3受热易分解为I2,而I2受热易升华.为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是AC.
A.Na2S2O3B.AlCl3C.Na2CO3D.NaNO2.
分析 (1)碘是紫黑色固体;加热时碘易升华.
(2)KIO3在酸性介质中与过氧化氢作用生成单质碘和氧气;
(3)电解时,阳极上发生氧化反应,碘离子在阳极上失去电子结合氢氧根生成碘酸根离子;
(4)KI溶液在硫酸提供的酸性环境下,被氧气氧化成单质碘,碘单质遇到淀粉变蓝,通常利用此性质检验碘,从而判断反应速率的快慢;
(5)根据KI具有还原性及氧化还原反应、KI3在常温下不稳定性来分析;根据提高加碘盐(添加KI)的稳定性,主要是防止I- 被氧化来分析;为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失,所以稳定剂是和碘化钾不反应的物质.
解答 解:(1)碘是紫黑色固体;加热条件下碘易升华,杂质不易升华,所以采用升华的方法分离碘单质,故答案为:紫黑色;升华;
(2)KIO3在酸性介质中与过氧化氢作用生成单质碘和氧气,+5价碘元素降低生成碘单质,-1价的氧升高生成氧气,该反应的离子反应方程式为2IO3-+2H++5H2O2=I2↓+5O2↑+6H2O,故答案为:2IO3-+2H++5H2O2=I2↓+5O2↑+6H2O;
(3)电解时,阳极上发生氧化反应,碘离子向阳极移动,在阳极上失去电子生成碘酸根离子,电极反应式为I-+6OH--6e-=IO3-+3H2O,所以阴极的阴离子氢氧根要移向阳极,所以图中的序号3应为阴离子交换膜,故答案为:阴;I-+6OH--6e-=IO3-+3H2O;
(4)KI溶液在硫酸提供的酸性环境下,被氧气氧化成单质碘,碘单质遇到淀粉变蓝,通常利用此性质检验碘,从而判断反应速率的快慢,所以应先加入淀粉溶液,后加入0.1mol/LH2SO4溶液,反应的离子方程式为:4H++4I-+O2=2I2+2H2O,故答案为:淀粉溶液;0.1mol/LH2SO4溶液;4H++4I-+O2=2I2+2H2O;
(5)KI作为加碘剂的食盐在保存过程中,KI会被空气中氧气氧化,KI在潮湿空气中氧化的反应化学方程式为:4KI+O2+2H2O═2I2+4KOH,根据题目告知,KI3•H2O是在低温条件下,由I2溶于KI溶液可制得.再由题给的信息:“KI+I2?KI3”,可知KI3在常温下不稳定性,低温条件下易分解为KI和I2,KI又易被空气中的氧气氧化,I2易升华,所以KI3•H2O作为食盐加碘剂是不合适的;提高加碘盐(添加KI)的稳定性,主要是防止I- 被氧化,根据题给信息“还原性:S2O32->I-”和氧化还原反应的强弱规律,可以选Na2S2O3作稳定剂;又由题给信息“3I2+6OH-═IO3-+5I-+3H2O”,可知I2与OH-会发生反应生成IO3-和5I-,而Na2CO3水解呈碱性,因而也可以用Na2CO3作稳定剂,防止加碘盐(添加KI)在潮湿环境下被氧气氧化.至于AlCl3,水解后呈酸性,且还原性I->Cl-,所不能作稳定剂;NaNO2当遇强还原性物质时能表现出氧化性,则NaNO2与KI能发生氧化还原反应为2NO2-+2I-+4H+=2NO↑+I2+2H2O,所以不能作稳定剂,
故答案为:否;低温制备的KI3受热易分解为I2,而I2受热易升华;AC.
点评 本题考查了碘的物理性质、电解原理、碘离子的检验等性质,难度不大,明确酸性条件下碘离子和碘酸根离子能生成碘单质,碱性条件下,碘能和氢氧根离子生成碘离子和碘酸根离子.

| A. | 乙醇的球棍模型为: | B. | 次氯酸的结构式为:H一C1一O | ||
| C. | 淀粉的结构简式为:[C6H12O6]n | D. | 乙烯的电子式为: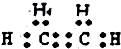 |
| A. | CH2=CH(CH2)2CH3 | B. | CH2=CH(CH2)3CH3 | ||
| C. | CH3CH=CHCH=CHCH3 | D. | CH3CH2CH=CHCH2CH3 |
| A. | CH4和NH3 | B. | N2和CO | C. | NH2-和H3O+ | D. | HCl和H2O |
| A. | C60与金刚石一样属于原子晶体 | |
| B. | 水结冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| C. | 分子晶体中必含化学键 | |
| D. | 干冰升华破坏了共价键 |
| A. | CH4 | B. | CO2 | C. | H2O | D. | NH3 |