题目内容
下列关于pH=3的盐酸和醋酸溶液的说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量分别为a和b,则a<b |
| C、加入足量的铁粉,放出H2的体积相同 |
| D、分别用蒸馏水稀释m倍和n倍,两溶液pH仍相同,则m=n |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氯化氢是强电解质,醋酸是弱电解质,存在电离平衡,pH相同的盐酸和醋酸,盐酸的浓度小于醋酸,加水稀释促进醋酸的电离,以此解答.
解答:
解:A.酸电离出氢离子抑制水的电离,pH=3的盐酸和醋酸溶液中氢离子浓度相同,对水的抑制程度相同,所以水电离出来的c(H+)相同,故A错误;
B.由于氯化氢是强电解质,醋酸是弱电解质,故pH=3的两种溶液中,醋酸浓度大,则中和相同体积的两种酸溶液,则醋酸所需NaOH的物质的量较大,故B正确;
C.pH=3的两种溶液中,醋酸浓度大,但由于两溶液体积大小关系不明确,故醋酸和盐酸的物质的量的大小关系不明确,与足量的铁粉反应时放出的氢气的体积不一定相同,故C错误;
D.分别用蒸馏水稀释m倍和n倍,醋酸进一步电离,氢离子浓度较大,若稀释后两溶液pH仍相同,则醋酸中加水较多,则m<n,故D错误.
故选B.
B.由于氯化氢是强电解质,醋酸是弱电解质,故pH=3的两种溶液中,醋酸浓度大,则中和相同体积的两种酸溶液,则醋酸所需NaOH的物质的量较大,故B正确;
C.pH=3的两种溶液中,醋酸浓度大,但由于两溶液体积大小关系不明确,故醋酸和盐酸的物质的量的大小关系不明确,与足量的铁粉反应时放出的氢气的体积不一定相同,故C错误;
D.分别用蒸馏水稀释m倍和n倍,醋酸进一步电离,氢离子浓度较大,若稀释后两溶液pH仍相同,则醋酸中加水较多,则m<n,故D错误.
故选B.
点评:本题考查了强酸弱酸的电离、溶液pH的变化分析、影响弱电解质电离平衡的因素,易错选项是C,注意生成氢气的量与溶液中酸的物质的量有关,题目难度不大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
下列叙述错误的是( )
①糯米中的淀粉一经发生水解反应,就生成酒精
②蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解
③纤维素属于天然高分子化合物,一切植物均含有纤维素
④石油裂化的主要目的是为了生产乙烯、丙烯等有机化工原料
⑤乙醇在一定条件下可被氧化为乙醛.
①糯米中的淀粉一经发生水解反应,就生成酒精
②蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解
③纤维素属于天然高分子化合物,一切植物均含有纤维素
④石油裂化的主要目的是为了生产乙烯、丙烯等有机化工原料
⑤乙醇在一定条件下可被氧化为乙醛.
| A、④⑤ | B、②③ | C、①④ | D、①②④ |
下列离子方程式正确的是( )
| A、铝与氢氧化钠溶液反应:2Al+2OH-+H2O═2[Al(OH)4]-+H2↑ |
| B、过氧化钠与水反应:2O2-+2H2O=4OH-+O2↑ |
| C、把少量碳酸氢钠溶液加入到氢氧化钡溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D、金属铜跟浓硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO2↑+4H2O |
环境污染已成为人类社会面临的重大威胁,下列名词与环境污染有关的是( )
(1)酸雨 (2)臭氧空洞 (3)白色污染 (4)温室效应 (5)赤潮 (6)光化学烟雾.
(1)酸雨 (2)臭氧空洞 (3)白色污染 (4)温室效应 (5)赤潮 (6)光化学烟雾.
| A、只有(1)(3)(4)(5) |
| B、只有(1)(2)(3)(4)(6) |
| C、只有(3)(4)(5)(6) |
| D、全部 |
根据水溶液中存在的平衡关系,判断下列说法正确的是( )
| A、往水中滴加少量稀硫酸,能促进水电离 |
| B、室温下,稀释0.1mol?L-1的醋酸,溶液中所有离子的浓度均降低 |
| C、往AgCl悬浊液中加入0.1mol?L-1Na2S溶液,有黑色沉淀产生 |
| D、浓度均为0.1 mol?L-1的溶液,pH由大到小排列顺序为:NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
纳米钴(Co)加氢反应的催化剂,500K时催化反应:CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0.有关说法正确的是( )
| A、纳米技术的应用,提高了催化剂酌催化性能,但平衡常数不变? |
| B、缩小容器体积,平衡向正反应方向移动CO的浓度减小? |
| C、温度越低,越有利于CO催化加氢 |
| D、从平衡体系中分H2O(g)能加快正反应速率? |
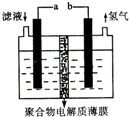 将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )
将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )| A、过滤得到的沉淀可能是FeS和S |
| B、若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C、可以用Fe与外接电源的a极相连 |
| D、与a极相连的电极反应为Fe2+-e-=Fe3+ |


 ,标明每一部的反应物及反应条件(有机物写结构简式,其他原料自选 )
,标明每一部的反应物及反应条件(有机物写结构简式,其他原料自选 )