题目内容
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,B元素的最高正价和最低负价之和为2.又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体.请回答下列问题:
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是 (用离子符号表示).
(2)由A、B两种元素以原子个数比5:1形成离子化合物X,X的电子式为 .
(3)由A、B元素形成的化合物B2A4可以与O2、KOH溶液形成原电池,该原电池负极的电极反应式为 .
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出该反应的化学方程式: .
(5)由A、C、D、F四种元素形成的化合物Y(DAFC3)(已知A2FC3的Ka1=1.3×10-2、Ka2=6.3×10-8),则Y溶液中各离子浓度由大到小的顺序为 ;室温下,向Y溶液中加入一定量的NaOH,使溶液中c(AFC3-)=c(FC32-),则此时溶液呈 (填“酸性”、“碱性”或“中性”).
(6)A 和B 形成的某种氯化物BA2Cl 可作杀菌剂,其原理为BA2Cl 遇水反应生成一种具有强氧化性的含氧酸,写出BA2Cl 与水反应的化学方程式: .
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是
(2)由A、B两种元素以原子个数比5:1形成离子化合物X,X的电子式为
(3)由A、B元素形成的化合物B2A4可以与O2、KOH溶液形成原电池,该原电池负极的电极反应式为
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出该反应的化学方程式:
(5)由A、C、D、F四种元素形成的化合物Y(DAFC3)(已知A2FC3的Ka1=1.3×10-2、Ka2=6.3×10-8),则Y溶液中各离子浓度由大到小的顺序为
(6)A 和B 形成的某种氯化物BA2Cl 可作杀菌剂,其原理为BA2Cl 遇水反应生成一种具有强氧化性的含氧酸,写出BA2Cl 与水反应的化学方程式:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:C元素的原子最外层电子数是次外层电子数的三倍,且是短周期元素,所以C是O元素,C与F同主族,且是短周期元素,所以F是S元素,B元素的最高正价和最低负价之和为2,B的原子序数小于C,且B、C处于同一周期,所以B是N元素,D与E和F同周期,都处于第三周期,E是金属元素,其单质与氧化铁反应常用于焊接钢轨,则E为Al元素,六种元素所形成的常见单质在常 温常压下有三种是气体,三种是固体,根据已经判断出来的元素可知,B、C的单质是气态,E、F的单质是固态,所以A、D对应的单质为一个固态、一个气态,且A与D同主族,D在第三周期,原子序数小于铝,A的原子序数小于氮,可推知A是H元素,D是Na元素,据此答题.
解答:
解:C元素的原子最外层电子数是次外层电子数的三倍,且是短周期元素,所以C是O元素,C与F同主族,且是短周期元素,所以F是S元素,B元素的最高正价和最低负价之和为2,B的原子序数小于C,且B、C处于同一周期,所以B是N元素,D与E和F同周期,都处于第三周期,E是金属元素,其单质与氧化铁反应常用于焊接钢轨,则E为Al元素,六种元素所形成的常见单质在常 温常压下有三种是气体,三种是固体,根据已经判断出来的元素可知,B、C的单质是气态,E、F的单质是固态,所以A、D对应的单质为一个固态、一个气态,且A与D同主族,D在第三周期,原子序数小于铝,A的原子序数小于氮,可推知A是H元素,D是Na元素,
(1)离子电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,O、Na离子电子层结构相同且Na元素原子序数大于O元素,所以离子半径:O2->Na+,S离子核外有3个电子层,O、Na离子核外有2个电子层,所以O、Na、S三种元素形成的简单离子的半径由大到小的顺序是:S2->O2->Na+,
故答案为:S2->O2->Na+;
(2)由H、N两种元素以原子个数比5:1形成离子化合物NH4H,该化合物中氢离子和铵根离子之间存在离子键、铵根离子中N原子和H原子之间存在共价键,X的电子式为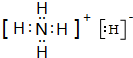 ,
,
故答案为: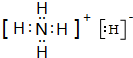 ;
;
(3)由H、N元素形成的化合物N2H4可以与O2、KOH溶液形成原电池,原电池中负极上燃料失电子发生氧化反应生成氮气和水,电极反应式为N2H4-4e-+4OH-=N2+4H2O,
故答案为:N2H4-4e-+4OH-=N2+4H2O;
(4)高温下,铝和氧化铁发生置换反应生成氧化铝和铁,反应方程式为2Al+Fe2O3
2Fe+Al2O3,
故答案为:2Al+Fe2O3
2Fe+Al2O3;
(5)由H、O、Na、S四种元素形成的化合物Y(NaHSO3),已知H2SO3的Ka1=1.3×10-2、Ka2=6.3×10-8,所以HSO3-的水解平衡常数为
=1.6×10-5<Ka1,故HSO3- 的电离程度大于水解程度,溶液呈酸性,但水解和电离程度都较小,所以溶液中离子浓度大小顺序是c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);向Y溶液中加入一定量的NaOH,使溶液中c(HSO3-)=c(SO32-),亚硫酸根离子水解程度大于亚硫酸氢根离子电离程度,所以溶液呈碱性,
故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);碱性;
(6)A 和B 形成的某种氯化物为NH2Cl 可作杀菌剂,其原理为NH2Cl 遇水反应生成一种具有强氧化性的含氧酸为次氯酸,NH2Cl 与水反应的化学方程式为NH2Cl+H2O=HClO+NH3,
故答案为:NH2Cl+H2O=HClO+NH3.
(1)离子电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,O、Na离子电子层结构相同且Na元素原子序数大于O元素,所以离子半径:O2->Na+,S离子核外有3个电子层,O、Na离子核外有2个电子层,所以O、Na、S三种元素形成的简单离子的半径由大到小的顺序是:S2->O2->Na+,
故答案为:S2->O2->Na+;
(2)由H、N两种元素以原子个数比5:1形成离子化合物NH4H,该化合物中氢离子和铵根离子之间存在离子键、铵根离子中N原子和H原子之间存在共价键,X的电子式为
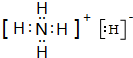 ,
,故答案为:
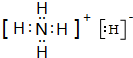 ;
;(3)由H、N元素形成的化合物N2H4可以与O2、KOH溶液形成原电池,原电池中负极上燃料失电子发生氧化反应生成氮气和水,电极反应式为N2H4-4e-+4OH-=N2+4H2O,
故答案为:N2H4-4e-+4OH-=N2+4H2O;
(4)高温下,铝和氧化铁发生置换反应生成氧化铝和铁,反应方程式为2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
(5)由H、O、Na、S四种元素形成的化合物Y(NaHSO3),已知H2SO3的Ka1=1.3×10-2、Ka2=6.3×10-8,所以HSO3-的水解平衡常数为
| KW |
| Ka2 |
故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);碱性;
(6)A 和B 形成的某种氯化物为NH2Cl 可作杀菌剂,其原理为NH2Cl 遇水反应生成一种具有强氧化性的含氧酸为次氯酸,NH2Cl 与水反应的化学方程式为NH2Cl+H2O=HClO+NH3,
故答案为:NH2Cl+H2O=HClO+NH3.
点评:本题考查位置结构性质的相互关系及应用,涉及离子浓度大小比较、铝热反应、电子式等知识点,侧重考查基本理论和化学用语,熟练掌握盐类水解等知识点,题目难度中等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
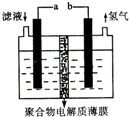 将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )
将H2S通人FeCl3溶液中,过滤后将反应液加人电解槽中电解(如图所示)电解后的溶液还可以循环利用.该方法可用于处理石油炼制过程中产生的H2S废气.下列有关说法正确的是( )| A、过滤得到的沉淀可能是FeS和S |
| B、若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C、可以用Fe与外接电源的a极相连 |
| D、与a极相连的电极反应为Fe2+-e-=Fe3+ |
如表为元素周期表短周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )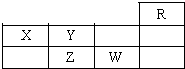

| A、常压下五种元素的单质中W单质的沸点最高 |
| B、Z的氢化物比Y的氢化物稳定 |
| C、W元素最高价氧化物的水化物酸性比Z元素的强 |
| D、Z、W的阴离子电子层结构与R原子的相同 |
进行中和滴定时,事先不应该用所盛溶液洗涤的仪器是( )
| A、酸式滴定管 | B、碱式滴定管 |
| C、锥形瓶 | D、移液管 |
下列溶液加热蒸干后,能析出溶质固体的是( )
| A、AlCl3 |
| B、KHCO3 |
| C、硫酸铁 |
| D、NH4HCO3 |


 ,标明每一部的反应物及反应条件(有机物写结构简式,其他原料自选 )
,标明每一部的反应物及反应条件(有机物写结构简式,其他原料自选 ) 实验室有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
实验室有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.