题目内容
 如图所示是某化学小组根据教材知识设计,说明Na2CO3与NaHCO3热稳定性的套管实验.下列叙述中不正确的是( )
如图所示是某化学小组根据教材知识设计,说明Na2CO3与NaHCO3热稳定性的套管实验.下列叙述中不正确的是( )| A、甲为NaHCO3,乙为Na2CO3 |
| B、要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球 |
| C、加热不久就能看到A烧杯中的澄清石灰水变浑浊 |
| D、整个实验过程中A烧杯中的澄清石灰水无明显变化 |
考点:探究碳酸钠与碳酸氢钠的性质
专题:
分析:A.碳酸氢钠不稳定,受热易分解,碳酸钠受热不分解,结合图中装置可知,乙受热温度高,应该为碳酸钠;
B.白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体,据此可以检验是否有水生成;
C.碳酸钠不分解,则A烧杯中不会出现浑浊现象,应该是B烧杯中的澄清石灰水出现浑浊现象;
D.由于碳酸钠稳定性较强,加热过程中不分解,则整个过程中A烧杯中的澄清石灰水不会变浑浊.
B.白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体,据此可以检验是否有水生成;
C.碳酸钠不分解,则A烧杯中不会出现浑浊现象,应该是B烧杯中的澄清石灰水出现浑浊现象;
D.由于碳酸钠稳定性较强,加热过程中不分解,则整个过程中A烧杯中的澄清石灰水不会变浑浊.
解答:
解:A.碳酸氢钠不稳定,受热易分解,碳酸钠受热不分解,结合图中装置可知,乙受热温度高,为说明碳酸氢钠不稳定,则应在较低温度下分解,则甲中应为NaHCO3,乙为Na2CO3,故A正确;
B.白色的无水硫酸铜与水反应会生成蓝色的硫酸铜晶体,所以要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球,故B正确;
C.NaHCO3不稳定,加热易分解:2NaHCO3
Na2CO3+CO2↑+H2O,所以B烧杯中的澄清石灰水变浑浊,而碳酸钠加热不分解,则烧杯A的澄清石灰水不会变浑浊,故C错误;
D.由于碳酸钠不分解,则整个过程中烧杯A中的澄清石灰水不会变浑浊,故D正确;
故选C.
B.白色的无水硫酸铜与水反应会生成蓝色的硫酸铜晶体,所以要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球,故B正确;
C.NaHCO3不稳定,加热易分解:2NaHCO3
| ||
D.由于碳酸钠不分解,则整个过程中烧杯A中的澄清石灰水不会变浑浊,故D正确;
故选C.
点评:本题考查Na2CO3和NaHCO3性质的异同,侧重于基础知识的考查与运用,为高频考点,题目难度不大,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累.

练习册系列答案
相关题目
己烯雌酚是一种激素类药物,结构如下列叙述中正确的是( )
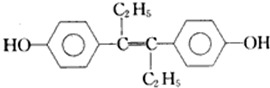

| A、该有机物分子中,最多可能有18个碳原子共平面 |
| B、该分子中有7个碳碳双键,可以与氢气1:7加成 |
| C、该分子对称性好,所以没有顺反异构 |
| D、标况下,1mol该有机物与足量金属钠反应可以放出22.4L的氢气 |
当Mg(OH)2在水中达到溶解平衡时:Mg(OH)2?Mg2++2OH- 要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是( )
| A、NH4Cl |
| B、NaOH |
| C、Na2CO3 |
| D、干冰 |
下列物质:①H3O+ ②[B(OH)4]- ③CH3COO ④NH3 ⑤CH4⑥NH4+中存在配位键的是( )
| A、①②⑥ | B、①③⑤ |
| C、③④⑤ | D、②④⑥ |
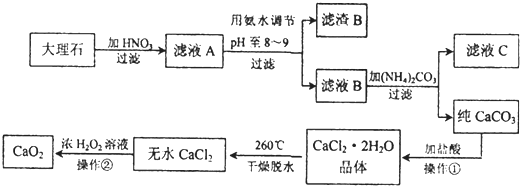
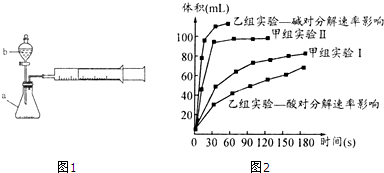
 某化学课外活动小组从实验室取出硫酸试剂,试剂瓶上标签的部分内容如图所示.该小组欲配制450mL 0.4mol?L-1的稀硫酸溶液:
某化学课外活动小组从实验室取出硫酸试剂,试剂瓶上标签的部分内容如图所示.该小组欲配制450mL 0.4mol?L-1的稀硫酸溶液: