��Ŀ����
13��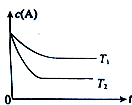 ������ѧ֪ʶ������������⣺
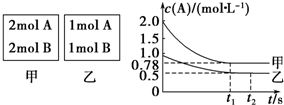
������ѧ֪ʶ������������⣺��ӦA��g��?B��g��+C��g�����ݻ�Ϊ1.0L���ܱ������н��У�A�ij�ʼŨ��Ϊ0.050mol/L���¶�T1��T2��A��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺
��1��������Ӧ���¶�T1С�� T2��ƽ�ⳣ��K��T1��С��K��T2����������ڡ�����С�ڡ����ڡ���
��2�����¶�T2ʱ��5min��Ӧ�ﵽƽ�⣬A��ת����Ϊ70%����
��ƽ��ʱ��ϵ�ܵ����ʵ���Ϊ0.085mol��
�ڷ�Ӧ��ƽ�ⳣ��K=0.082�������������λ��Ч���֣�
�۷�Ӧ��0��5min�����ƽ����Ӧ����v��A��=0.007mol/��L•min����
��3���ϳɰ����Ȼ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1
��֪��

1mol N-H���������յ�����Ϊ391kJ��
��4��������������ȼ�ϵ�ص�ȼ�ϣ���ط�ӦΪ 4NH3+3O2=2N2+6H2O����ȼ�ϵ�صĸ����缫��ӦΪ2NH3-6e-+6OH-=N2+6H2O��
���� ��1���¶�Խ�ߴ�ƽ�������ʱ��Խ�̣�Ȼ����ͼ�������Ӧ����ЧӦ���Ӷ��ó�K�ı仯�����
��2����������ʽ�����ƽ�ⳣ���ͷ�Ӧ���ʵĹ�ʽ����⣮
��3����ѧ��Ӧ�ɼ����������������¼������ͷ���������Ӧ�ʱ����ֵ�����������IJ�ֵ��
��4����ȼ�ϵ���У���������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
��� �⣺��1����ͼ��֪T2�ȴ�ƽ��״̬������T1С��T2�����¶�Խ��KԽС����������ӦΪ���ȷ�Ӧ�������¶�Խ��KֵԽ�ʴ�Ϊ��С�ڣ�С�ڣ�
��2��A��g��?B��g��+C��g��
��ʼŨ�ȣ�0.050 0 0
�仯Ũ�ȣ�0.035 0.035 0.035
ƽ��Ũ�ȣ�0.015 0.035 0.035
��ƽ��ʱ��ϵ�ܵ����ʵ���Ϊ=��0.015+0.035+0.035����1=0.085mol��
��K=$\frac{0.035��0.035}{0.015}$=0.082��
�۷�Ӧ��0��5min�����ƽ����Ӧ����v��A��=$\frac{0.035mol/L}{5min}$=0.007mol/��L•min����
�ʴ�Ϊ��0.085mol��0.082��0.007mol/��L•min����
��3����Ӧ�ȵ��ڷ�Ӧ����ܼ��ܼ�ȥ��������ܼ��ܣ�����N2��g��+3H2��g��?2NH3��g����H=-92.2kJ•mol-1����N-H����Ϊ xKJ/mol����945.8kJ/mol+3��436kJmol-6xkJ/mol=-92.2kJ/mol���x=391���ʴ�Ϊ��391��
��4��������������ȼ�ϵ�ص�ȼ�ϣ����ݵ�ط�Ӧ��4NH3+3O2�T2N2+6H2O����ȼ�ϵ�صĸ�������ȼ�ϰ�������ʧ���ӵ�������Ӧ����缫��Ӧ2NH3-6e-+6OH-=N2+6H2O���ʴ�Ϊ��2NH3-6e-+6OH-=N2+6H2O��
���� ���⿼���˻�ѧ��Ӧ�����仯����ѧƽ��Ӱ�����صķ����жϣ�ͼ������뻯ѧƽ��ļ���Ӧ�ã�Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬��Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ʯī | B�� | �������� | C�� | п | D�� | �� |

��֪��
��һ����ͬ�¶���H3BO3���ܽ��
| ���¶ȣ��棩 | ��20 | ��40 | ��60 | ��100 |
| ���ܽ�ȣ�g�� | ��5.0 | ��8.7 | ��14.8 | ��40.2 |
| ������������ | ��Fe��OH��3 | ��Al��OH��3 | ��Fe��OH��2 | ��Mg��OH��2 |
| ��pH | ��3.2 | ��5.2 | ��9.7 | ��12.4 |
��2������ȡ��ʱΪ������ʣ����ʵ���������Ũ���⣬���ɲ�ȡ�Ĵ�ʩ����߷�Ӧ�¶ȣ�����ȡ�����á��ȹ��ˡ���Ŀ��Ϊ��ֹ���¶��½�ʱH3BO3����Һ��������
��3��������Һ�������ԣ�����H3BO3��Mg2+��������Fe2+��Fe3+��Ca2+��Al3+�����ʣ������ӡ�ʱ�������Һ�����μ���������H2O2��MgO�����Գ�ȥ����������ΪFe3+��Fe2+��Al3+��H2O2������ΪH2O2+2H++2Fe2+=2Fe3++2H2O�������ӷ���ʽ��ʾ����
��4����ĸҺ�������ڻ�������þ����֪����þ���ܽ�����¶ȱ仯��������ͼ��ʾ������Һ�ķе���ѹǿ��������ߣ�Ϊ�˴ӡ�ĸҺ���г�ֻ���MgSO4•H2O��Ӧ��ȡ�Ĵ�ʩ�ǽ���ĸҺ������Ũ������ѹ�����½ᾧ�����ˣ�
��5����֪25��ʱ�����ᣨH3BO3����Һ�д�������ƽ�⣺H3BO3��aq��+H2O��l��?[B��OH��4]-��aq��+H+��aq�� K=5.7��10-10.25��ʱ��0.7mol/L������Һ��c��H+��=2��10-5mol/L
��6����֪25��ʱ��
| ��ѧʽ | H2CO3 | HF |
| ���볣�� | K1=4.4��10-7 K2=4.7��10-11 | K=6.75��10-4 |
A��̼������Һ����������Һ�й۲쵽�����ݲ���
B��̼������Һ����������й۲쵽�����ݲ���
C����Ũ��̼����Һ��������Һ��pH��ǰ�ߣ�����
D����Ũ��̼������Һ�ͷ�������Һ��pH��ǰ�ߣ����ߣ�
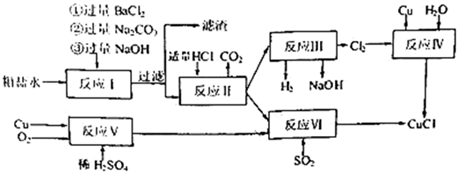
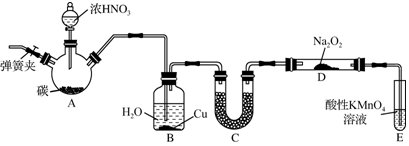
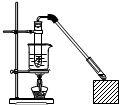 ������Ҵ���Ӧ��װ����ͼ��ʾ�����Թ������3mL�Ҵ���Ȼ��һ��ҡ����һ�������ؼ���2mLŨ�����2mL�����ᣬ�þƾ���С�ľ��ȵؼ���10min����������������������ͨ�뵽����̼������Һ��Һ���ϣ�
������Ҵ���Ӧ��װ����ͼ��ʾ�����Թ������3mL�Ҵ���Ȼ��һ��ҡ����һ�������ؼ���2mLŨ�����2mL�����ᣬ�þƾ���С�ľ��ȵؼ���10min����������������������ͨ�뵽����̼������Һ��Һ���ϣ�