题目内容
设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、常温常压下,32gO2和O3的混合气体所含原子数为2NA |
| B、1.8g重水(D2O)中含NA个中子 |
| C、标准状况下11.2L乙醇中含0.5NA个乙醇分子 |
| D、8gCuSO4 溶于水中配成0.1mol/L的溶液500ml |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氧气和臭氧分子中都只含有氧原子,32g混合物中含有32g氧原子;
B.重水中含有10个中子,重水的摩尔质量为20g/mol;
C.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
D.根据n=cV计算出硫酸铜的物质的量,再根据m=nM计算出硫酸铜的质量.
B.重水中含有10个中子,重水的摩尔质量为20g/mol;
C.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
D.根据n=cV计算出硫酸铜的物质的量,再根据m=nM计算出硫酸铜的质量.
解答:
解:A.32g氧气和臭氧的混合物中含有32g氧原子,含有2mol氧原子,混合气体所含原子数为2NA,故A正确;
B.1.8g重水的物质的量为:
=0.09mol,含有中子的物质的量为:10×0.09mol=0.9mol,含0.9NA个中子,故B错误;
C.标况下,乙醇为液体,不能使用标况下的气体摩尔体积计算11.2L乙醇的物质的量,故C错误;
D.500mL 0.1mol/L的硫酸铜溶液中含有硫酸铜的质量为:m=0.1mol/L×0.5L×160g/mol=8.0g,可以用8g硫酸铜溶于水配制500mL 0.1mol/L的硫酸铜溶液,故D正确;
故选AD.
B.1.8g重水的物质的量为:
| 1.8g |
| 20g/mol |
C.标况下,乙醇为液体,不能使用标况下的气体摩尔体积计算11.2L乙醇的物质的量,故C错误;
D.500mL 0.1mol/L的硫酸铜溶液中含有硫酸铜的质量为:m=0.1mol/L×0.5L×160g/mol=8.0g,可以用8g硫酸铜溶于水配制500mL 0.1mol/L的硫酸铜溶液,故D正确;
故选AD.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下乙醇的状态不是气体,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意重水摩尔质量为20g/mol.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2 L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1 mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
设NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
下列实验操作中所用仪器合理的是( )
| A、用25 mL的碱式滴定管量取14.80mLH2SO4溶液 |
| B、用100 mL量筒量取5.2 mL盐酸 |
| C、用托盘天平称取25.2g氯化钠 |
| D、用100 mL容量瓶配制50 mL 0.1 mol/L盐酸 |
下列物质:①水泥 ②玻璃 ③陶瓷 ④水晶,其中属于硅酸盐工业产品的是( )
| A、只有①② | B、只有②④ |
| C、只有①②③ | D、全部 |
下面说法正确的是( )
| A、C60是一种新型的化合物 |
| B、C60和石墨物理性质不同 |
| C、C60分子不能与氧气反应 |
| D、C60的摩尔质量是720 |
以下实验操作正确的是( )
A、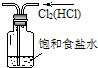 除去Cl2中的HCl气体 |
B、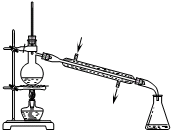 淡化海水 |
C、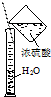 稀释浓硫酸 |
D、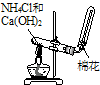 验室制取氨气 |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42-=0.2mol/L,当加等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的浓度是( )
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.45 mol/L |
| D、0.225 mol/L |