题目内容
设NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.甲烷分子中含有质子数、电子数都是10;
B.醋酸为弱酸,溶液中只能部分电离出氢离子,溶液中氢离子物质的量一定小于0.1mol;
C.镁原子最外层为2个电子,1mol镁原子含有2mol最外层电子;
D.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算乙醇的物质的量.
B.醋酸为弱酸,溶液中只能部分电离出氢离子,溶液中氢离子物质的量一定小于0.1mol;
C.镁原子最外层为2个电子,1mol镁原子含有2mol最外层电子;
D.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算乙醇的物质的量.
解答:
解:A.1mol甲烷分子中含有的中子、质子的物质的量都是10mol,所含质子数、电子数均为10NA,故A正确;
B.1L0.1mol/L乙酸溶液中含有溶质醋酸0.1mol,由于醋酸为弱电解质,则溶液中氢离子小于0.1mol,H+离子数小于0.1NA,故B错误;
C.24g镁原子的物质的量为1mol,1mol镁原子含有的最外层电子为2mol,含有的最外层电子数为2NA,故C错误;
D.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算22.4L乙醇的物质的量,故D错误;
故选A.
B.1L0.1mol/L乙酸溶液中含有溶质醋酸0.1mol,由于醋酸为弱电解质,则溶液中氢离子小于0.1mol,H+离子数小于0.1NA,故B错误;
C.24g镁原子的物质的量为1mol,1mol镁原子含有的最外层电子为2mol,含有的最外层电子数为2NA,故C错误;
D.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算22.4L乙醇的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |
用如图装置进行的实验,不能达到相应实验目的是( )
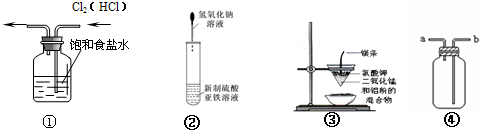

| A、装置①可除去Cl2中的HCl杂质 |
| B、装置②可用于制备氢氧化亚铁并观察其颜色 |
| C、装置③可制取金属锰 |
| D、装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体 |
关于体积相同、pH均为3的H2SO4溶液和CH3COOH溶液,下列说法正确的是( )
| A、分别与足量的Mg反应,CH3COOH溶液产生的H2多 |
| B、分别用pH=12的NaOH溶液中和,H2SO4消耗的NaOH多 |
| C、分别加入对应的钠盐固体后,二者pH仍为3 |
| D、分别加水稀释100倍后,二者的pH均变为5 |
用1L 1.0mol/L NaOH溶液吸收0.8mol C02,所得溶液中含有( )
| A、C032- |
| B、HC03- |
| C、C032-和HC03- |
| D、C032-和OH- |
下列有关实验的操作正确的是( )
| A、容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| C、为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满 CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部 |
| D、用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 |
设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、常温常压下,32gO2和O3的混合气体所含原子数为2NA |
| B、1.8g重水(D2O)中含NA个中子 |
| C、标准状况下11.2L乙醇中含0.5NA个乙醇分子 |
| D、8gCuSO4 溶于水中配成0.1mol/L的溶液500ml |
下列各反应,能用同一离子方程式表示的是( )
| A、氢氧化铜与盐酸、氢氧化铜与醋酸 |
| B、氯化钡溶液与硫酸铜溶液、氢氧化钡溶液与硫酸铜溶液 |
| C、氢氧化钡与稀硫酸、氢氧化钡与稀盐酸 |
| D、石灰石与稀硝酸、石灰石与稀盐酸 |