题目内容
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2 L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1 mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.亚铁离子和碘离子都能够被氯气氧化,根据亚铁离子和碘离子的物质的量计算出转移的电子数;
B.硫酸钾中阳离子为硫酸根离子,1mol硫酸根离子带有2mol负电荷;
C.过氧化钠中的阴离子为过氧根离子,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子;
D.丙烯和环丙烷的分子式都是C3H6,42g混合物中含有1molC3H6.
B.硫酸钾中阳离子为硫酸根离子,1mol硫酸根离子带有2mol负电荷;
C.过氧化钠中的阴离子为过氧根离子,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子;
D.丙烯和环丙烷的分子式都是C3H6,42g混合物中含有1molC3H6.
解答:
解:A.1molFeI2中含有1mol亚铁离子、2mol碘离子,与足量氯气反应,1mol亚铁离子失去1mol电子、2mol碘离子失去2mol电子,总共转移了3mol电子,转移的电子数为:3NA,故A错误;
B.2 L 0.5 mol?L-1硫酸钾溶液中含有溶质硫酸钾1mol,1mol硫酸钾中含有1mol硫酸根离子,含有2mol负电荷,阴离子所带电荷数为2NA,故B错误;
C.1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol阴阳离子,含离子总数为3NA,故C错误;
D.42g丙烯和环丙烷的混合物中含有1molC3H6分子,含有6molH原子,含有氢原子的个数为6NA,故D正确;
故选D.
B.2 L 0.5 mol?L-1硫酸钾溶液中含有溶质硫酸钾1mol,1mol硫酸钾中含有1mol硫酸根离子,含有2mol负电荷,阴离子所带电荷数为2NA,故B错误;
C.1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol阴阳离子,含离子总数为3NA,故C错误;
D.42g丙烯和环丙烷的混合物中含有1molC3H6分子,含有6molH原子,含有氢原子的个数为6NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确过氧化钠中含有的阴离子为过氧根离子,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列各组离子在指定条件下,一定能大量共存的是( )
| A、能使红色石蕊试纸显蓝色的溶液:K+、Na+、SO42-、C2O42- |
| B、能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| C、水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、SO3-、S2- |
| D、加入铝条有氢气放出的溶液:Na+、NH4+、Cl-、NO3- |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
下列关于Na2O和Na2O2的叙述正确的是( )
| A、都是白色固体 |
| B、都能和水反应形成强碱溶液 |
| C、都是碱性氧化物 |
| D、都是强氧化剂 |
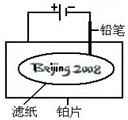 某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )
某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )| A、铅笔作阴极:电极反应为:2H++2e-=H2↑ | ||||
| B、铂片作阳极:电极反应为:2Cl--2e-=Cl2↑ | ||||
| C、铅笔与滤纸接触处有少量Cl2逸出 | ||||
D、上述反应总的离子方程式可表示为2Cl-+2H2O
|
进行化学实验、观察实验现象,通过分析、推理得出正确的结论是化学学习的方法之一.下列对有关实验事实的解释正确的是( )
| A、将N2和过量的O2在高温或放电的条件下反应得到红棕色的气体,说明NO为红棕色气体 |
| B、在AgNO3溶液中加入锌粉,能置换出银,说明Ag+的还原性比Zn2+强 |
| C、用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中含Na+ |
| D、浓硫酸放入蔗糖中,能使蔗糖炭化,说明浓硫酸具有脱水性 |
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |
用如图装置进行的实验,不能达到相应实验目的是( )
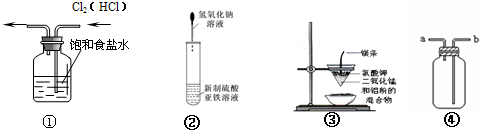

| A、装置①可除去Cl2中的HCl杂质 |
| B、装置②可用于制备氢氧化亚铁并观察其颜色 |
| C、装置③可制取金属锰 |
| D、装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体 |
设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、常温常压下,32gO2和O3的混合气体所含原子数为2NA |
| B、1.8g重水(D2O)中含NA个中子 |
| C、标准状况下11.2L乙醇中含0.5NA个乙醇分子 |
| D、8gCuSO4 溶于水中配成0.1mol/L的溶液500ml |