��Ŀ����
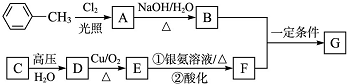
��֪�л���A��B��C��D��E��F��G����ͼ��ת����ϵ������C�IJ�������������һ�����ҵ�ʯ�ͻ�����չˮƽ��G�ķ���ʽΪC9H10O2���Իش������й����⣮
��1��G������Ϊ ��
��2��ָ�����з�Ӧ�ķ�Ӧ���ͣ�Aת��ΪB�� ��Cת��ΪD�� ��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��G������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ��
��4����������������G��ͬ���칹����ĿΪ �֣�
�ٱ�������3��ȡ��������������ȡ������ͬ�����ܹ������Ƶ�������Һ��Ӧ����������������
������ԭ�ӹ������ֲ�ͬ�������������ʵĽṹ��ʽΪ ��

��1��G������Ϊ
��2��ָ�����з�Ӧ�ķ�Ӧ���ͣ�Aת��ΪB��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��G������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��
��4����������������G��ͬ���칹����ĿΪ
�ٱ�������3��ȡ��������������ȡ������ͬ�����ܹ������Ƶ�������Һ��Ӧ����������������
������ԭ�ӹ������ֲ�ͬ�������������ʵĽṹ��ʽΪ
���㣺�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
������C�IJ�������������һ�����ҵ�ʯ�ͻ�����չˮƽ����CΪCH2=CH2����ˮ�����ӳɷ�Ӧ����DΪCH3CH2OH��D��������������EΪCH3CHO��E��������Һ����������Ӧ����FΪCH3COOH���ױ��������ڹ��������������ϵ�ȡ����Ӧ����A��A����ˮ�ⷴӦ����B��B��F��Ӧ����G��C9H10O2������G�ķ���ʽ��֪��BΪһԪ������AΪ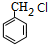 ��BΪ
��BΪ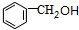 ��GΪ
��GΪ ���ݴ˽��
���ݴ˽��
 ��BΪ
��BΪ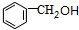 ��GΪ
��GΪ ���ݴ˽��
���ݴ˽�����
�⣺C�IJ�������������һ�����ҵ�ʯ�ͻ�����չˮƽ����CΪCH2=CH2����ˮ�����ӳɷ�Ӧ����DΪCH3CH2OH��D��������������EΪCH3CHO��E��������Һ����������Ӧ����FΪCH3COOH���ױ��������ڹ��������������ϵ�ȡ����Ӧ����A��A����ˮ�ⷴӦ����B��B��F��Ӧ����G��C9H10O2������G�ķ���ʽ��֪��BΪһԪ������AΪ ��BΪ
��BΪ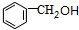 ��GΪ
��GΪ ��
��
��1��GΪ ������Ϊ���ᱽ�������ʴ�Ϊ�����ᱽ��������
������Ϊ���ᱽ�������ʴ�Ϊ�����ᱽ��������
��2��Aת��ΪB����ˮ�ⷴӦ��Cת��ΪD���ڼӳɷ�Ӧ���ʴ�Ϊ��ˮ�ⷴӦ���ӳɷ�Ӧ��
��3��G������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��4���������������� ��ͬ���칹�壺�ܹ������Ƶ�������Һ��Ӧ��������������������-CHO����������3��ȡ��������������ȡ������ͬ��������2��-CH3��
��ͬ���칹�壺�ܹ������Ƶ�������Һ��Ӧ��������������������-CHO����������3��ȡ��������������ȡ������ͬ��������2��-CH3��
2��-CH3���ڣ�-CHO��2��λ�ã�2��-CH3���ڼ�λ��-CHO��3��λ�ã�2��-CH3���ڶ�λ��-CHO��1��λ�ã��ʷ���������ͬ���칹����2+3+1=6�֣�������ԭ�ӹ������ֲ�ͬ�������������ʵĽṹ��ʽΪ�� ��
��
�ʴ�Ϊ��6�� ��
��
 ��BΪ
��BΪ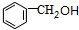 ��GΪ
��GΪ ��
����1��GΪ
 ������Ϊ���ᱽ�������ʴ�Ϊ�����ᱽ��������
������Ϊ���ᱽ�������ʴ�Ϊ�����ᱽ����������2��Aת��ΪB����ˮ�ⷴӦ��Cת��ΪD���ڼӳɷ�Ӧ���ʴ�Ϊ��ˮ�ⷴӦ���ӳɷ�Ӧ��
��3��G������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��
 ��
���ʴ�Ϊ��
 ��
����4����������������
 ��ͬ���칹�壺�ܹ������Ƶ�������Һ��Ӧ��������������������-CHO����������3��ȡ��������������ȡ������ͬ��������2��-CH3��
��ͬ���칹�壺�ܹ������Ƶ�������Һ��Ӧ��������������������-CHO����������3��ȡ��������������ȡ������ͬ��������2��-CH3��2��-CH3���ڣ�-CHO��2��λ�ã�2��-CH3���ڼ�λ��-CHO��3��λ�ã�2��-CH3���ڶ�λ��-CHO��1��λ�ã��ʷ���������ͬ���칹����2+3+1=6�֣�������ԭ�ӹ������ֲ�ͬ�������������ʵĽṹ��ʽΪ��
 ��
���ʴ�Ϊ��6��
 ��
��
���������⿼���л����ƶϣ��漰��������ȩ�������������ת���ȣ��ѶȲ����ǶԳ����л���֪ʶ�ļ����ã���4����ע�����á�������һ������дͬ���칹�壮

��ϰ��ϵ�д�
 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�
�����Ŀ
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A��NH4HSO4��Һ�м���������Ba��OH��2��Һ��OH-+H++Ba2++SO4-2=BaSO4��+H2O |
| B��С�մ���Һ�м���������Ca��OH��2��Һ��HCO3-+Ca2++OH-=CaCO3��+H2O |
| C����ϡ����ϴ���Թ��ڱ�������Ag+2H++NO3-=Ag++NO��+H2O |
| D����Mg��OH��2����Һ�еμ�FeCl3��Һ�����ɺ��ɫ������3OH-+Fe3+=Fe��OH��3�� |
����˵����ȷ���ǣ�������
| A����֪MgCO3��Ksp=6.82��10-6�������к��й���MgCO3����Һ�У�����c��Mg2+��=c��CO32-������c ��Mg2+��?c ��CO32-��=6.82��10-6 |
| B�������£���0.10 mol?L-1��NH3?H2O��Һ�м�������NH4Cl���壬c�� NH4+��/c��NH3?H2O��ֵ��� |
| C��pH=8.3��NaHCO3��Һ��c��Na+����c��HCO3-����c��CO32-����c ��H2CO3�� |
D��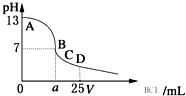 �����£���25 mL 0.1 mol?L-1NaOH��Һ����μ���0.2 mol?L-1HCl��Һ��pH��μ�HCl��Һ����Ĺ�ϵ������ͼ��ʾ�� �����£���25 mL 0.1 mol?L-1NaOH��Һ����μ���0.2 mol?L-1HCl��Һ��pH��μ�HCl��Һ����Ĺ�ϵ������ͼ��ʾ�� |
���з���������ԭ�Ӷ����������Ϊ8���ӽṹ���ǣ�������
| A��CCl4 |
| B��NO2 |
| C��PCl5 |
| D��NH3 |
 ���Ź����ͼ۲����������ϳ�CH3OH������͵��о���Ϊ�ȵ㣮
���Ź����ͼ۲����������ϳ�CH3OH������͵��о���Ϊ�ȵ㣮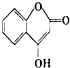 ��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�
��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�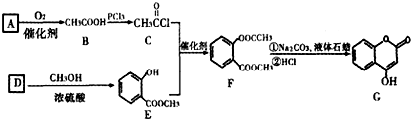
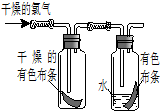 ��1����ͼ��ʾ������������ͨ��ʢ�и�����ɫ�����ĺ�ʢ�г�ʪ��ɫ�����Ĺ��ƿ���ɹ۲쵽��������
��1����ͼ��ʾ������������ͨ��ʢ�и�����ɫ�����ĺ�ʢ�г�ʪ��ɫ�����Ĺ��ƿ���ɹ۲쵽��������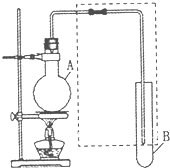 ��ͼ�����ڼ��л���������Ʊ������롢���ʱȽϵȵij�������װ�ã���
��ͼ�����ڼ��л���������Ʊ������롢���ʱȽϵȵij�������װ�ã���