题目内容
16.若在加入铝粉能放出氢气的溶液中,下列各组离子可能共存的是( )| A. | NH4+ NO3- CO32- Na+ | B. | Na+ Ba2+ Mg2+ HCO3- | ||
| C. | NO3- K+[Al(OH)4]- OH- | D. | NO3- Ba2+ K+ Cl- |
分析 加入铝粉能放出氢气的溶液呈酸性或强碱性,溶液中存在大量氢离子或氢氧根离子,
A.铵根离子与氢氧根离子反应,碳酸根离子与氢离子反应;
B.碳酸氢根离子与氢离子、氢氧根离子反应;
C.氢氧根离子与氢离子反应,[Al(OH)4]-与氢离子反应;
D.四种离子之间不反应,都不与氢离子、氢氧根离子反应.
解答 解:加入铝粉能放出氢气的溶液中存在大量氢离子或氢氧根离子,
A.NH4+与氢氧根离子,CO32-与氢离子反应,在溶液中一定不能大量共存,故A错误;
B.HCO3-与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故B错误;
C.OH-与氢离子反应,[Al(OH)4]-与氢离子反应,在溶液中一定不能大量共存,故C错误;
D.NO3-、Ba2+、K+、Cl-之间不发生反应,都不与氢离子和氢氧根离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
7.一定条件下硝酸铵受热分解的化学方程式为:3Cu+8HNO3=3Cu (NO3)2+2NO↑+4H2O,在反应中被还原与未被还原的氮原子数之比为( )
| A. | 8:3 | B. | 3:2 | C. | 1:3 | D. | 3:8 |
4.X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具行相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍.下列说法正确的是( )
| A. | X与Y形成的化合物只有一种 | |
| B. | 原子半径:r(Z)<r(R) | |
| C. | R的氯化物的热稳定性比W的强 | |
| D. | Y的最高价氧化物对应水化物的酸性比W的强 |
1.下列装置或操作能达到实验目的是( )
| A. |  制备氢氧化亚铁并观察其颜色 | B. |  构成铜锌原电池 | ||
| C. |  检查装置气密性 | D. |  浓硫酸稀释 |
5.设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2NA | |
| B. | 标准状况下,11.2 L CH3OH中含有的共价键数目为2.5NA | |
| C. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA | |
| D. | 常温常压下,16 g CH4中含有的原子总数为5NA |

 与NaOH的醇溶液共热制备CH3-CH=CH2.
与NaOH的醇溶液共热制备CH3-CH=CH2.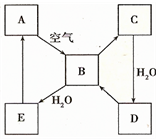 如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.
如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.