题目内容
6.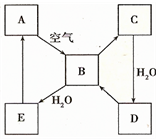 如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.
如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.I.单质A的名称硫.
II.写出D的浓溶液与Cu加热反应生成B的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 A能和空气反应生成B,且A是淡黄色固体,则A是S,B是SO2,B和C的相对分子质量相差16,说明B和C中相差一个O原子,则C是SO3,三氧化硫和水反应生成D,化合物D是重要的工业原料,所以D是H2SO4,B和水反应生成亚硫酸,所以E是H2SO3,结合物质的性质分析解答.
解答 解:A能和空气反应生成B,且A是淡黄色固体,则A是S,B是SO2,B和C的相对分子质量相差16,说明B和C中相差一个O原子,则C是SO3,三氧化硫和水反应生成D,化合物D是重要的工业原料,所以D是H2SO4,B和水反应生成亚硫酸,所以E是H2SO3,
I.通过以上分析知,A是硫单质,故答案为:硫;
II.在加热条件下,铜和浓硫酸发生氧化还原反应生成硫酸铜、二氧化硫和水,反应方程式为:Cu+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查了无机物的推断等知识点,根据A的颜色及物质间的反应来推断物质,明确物质的性质是解本题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.若在加入铝粉能放出氢气的溶液中,下列各组离子可能共存的是( )
| A. | NH4+ NO3- CO32- Na+ | B. | Na+ Ba2+ Mg2+ HCO3- | ||
| C. | NO3- K+[Al(OH)4]- OH- | D. | NO3- Ba2+ K+ Cl- |
17.反应C2H4(g)+3O2(g)═2CO2(g)+2H2O(g) 在四种不同情况下的反应速率分别为:
①v(C2H4)=0.45mol/(L•s)
②v(O2)=0.6mol/(L•s)
③v(CO2)=0.4mol/(L•s)
④v(H2O)=0.45mol/(L•s)
下列有关反应速率的比较中正确的是( )
①v(C2H4)=0.45mol/(L•s)
②v(O2)=0.6mol/(L•s)
③v(CO2)=0.4mol/(L•s)
④v(H2O)=0.45mol/(L•s)
下列有关反应速率的比较中正确的是( )
| A. | ①>②>③>④ | B. | ④>③>②>① | C. | ④>③=②>① | D. | ①>④>②=③ |
14.下列变化中,属于加成反应的是( )
| A. | 乙烯使酸性KMnO4溶液褪色的反应 | B. | 甲烷与氯气在光照条件下的反应 | ||
| C. | 乙烯使溴水褪色的反应 | D. | 乙烯的燃烧反应 |
11.有乙烯与乙炔的混合气体100mL,与280mL氧气充分反应,完全燃烧后生成二氧化碳的体积(以上气体体积均在相同状况下测定)
| A. | 小于200mL | B. | 200mL | C. | 大于200mL | D. | 无法确定 |
18.25℃时,某溶液中含有HCO${\;}_{3}^{-}$、SO${\;}_{3}^{2-}$、CO${\;}_{3}^{2-}$、CH3COO-四种阴离子,当向其中加入足量的Na2O2固体并降温至25℃后,下列有关溶液中离子浓度变化的说法错误的是(假设溶液的体积无变化)( )
| A. | CH3COO-的浓度基本不变 | |
| B. | SO${\;}_{3}^{2-}$的浓度减小,而SO${\;}_{4}^{2-}$的浓度增大 | |
| C. | CO${\;}_{3}^{2-}$的浓度减小,溶液碱性增强 | |
| D. | HCO${\;}_{3}^{-}$的浓度减,OH-的浓度增大 |
5.下列说法正确的是( )
| A. | 由不同原子组成的纯净物一定是化合物 | |
| B. | 一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,则该气体中每个分子含有2个原子 | |
| C. | 含金属元素的离子一定都是阳离子 | |
| D. | 胆矾是混净物,水泥是混合物 |
6.合成导电高分子材料PPV的反应:
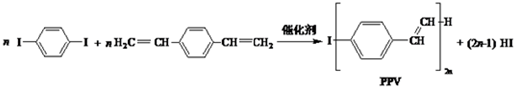
下列说法正确的是( )

下列说法正确的是( )
| A. | 合成PPV的反应为缩聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. | 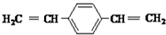 和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 通过红外光谱测定PPV的平均相对分子质量,可得其聚合度 |
 .
. .
.