题目内容
设NA代表阿佛加德罗常数的数值,下列说法中正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的中子数为8NA |
| B、64g的铜发生氧化还原反应,一定失去2 NA个电子 |
| C、常温常压22.4LNO气体的分子数为NA |
| D、标况时,22.4L三氯甲烷所含有的分子数为NA |
考点:阿伏加德罗常数
专题:
分析:A、依据n=
计算物质的量结合质子数+中子数=质量数计算中子数;
B、依据n=
计算物质的量,铜可以生成二价铜或一价铜;
C、依据气体摩尔体积应用条件分析,标准状况下气体摩尔体积为22.4L;
D、标准状况三氯甲烷不是气体.
| m |
| M |
B、依据n=
| m |
| M |
C、依据气体摩尔体积应用条件分析,标准状况下气体摩尔体积为22.4L;
D、标准状况三氯甲烷不是气体.
解答:
解:A、依据n=
计算物质的量=
=1mol,结合质子数+中子数=质量数计算中子数得到,中子数=1mol×(14+3×1-6-1×3)×NA=8NA,故A正确;
B、依据n=
计算物质的量=
=1mol,铜可以生成二价铜或一价铜,生氧化还原反应失去2NA个电子或NA个电子,故B错误;
C、依据气体摩尔体积应用条件分析,标准状况下气体摩尔体积为22.4L,常温常压22.4LNO气体物质的量不是1mol,故C错误;
D、标准状况三氯甲烷不是气体,22.4L三氯甲烷物质的量不是1mol,故D错误;
故选A.
| m |
| M |
| 17g |
| 17g/mol |
B、依据n=
| m |
| M |
| 64g |
| 64g/mol |
C、依据气体摩尔体积应用条件分析,标准状况下气体摩尔体积为22.4L,常温常压22.4LNO气体物质的量不是1mol,故C错误;
D、标准状况三氯甲烷不是气体,22.4L三氯甲烷物质的量不是1mol,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是氧化还原反应电子转移计算,气体摩尔体积概念的分析应用,掌握基础是关键,题目较简单.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
生物炼铜实际上是微生物帮助我们从矿石中提取铜.这些“吃岩石的细菌”能利用空气中的氧气将不溶性的CuS转化成可溶性铜的化合物,该化合物是( )
| A、碳酸铜 | B、硝酸铜 |
| C、硫酸铜 | D、氢氧化铜 |
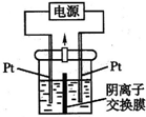 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )| A、右侧发生的电极方程式:2H2O+2e-=H2↑+2OH- | ||||
| B、电解结束时,右侧溶液中含有IO3- | ||||
C、电解槽内发生反应的总化学方程式KI+3H2O
| ||||
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |
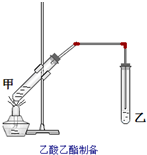 如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: