题目内容
7.含有0.20mol Na2CO3的溶液120mL和200mL 盐酸,不管将前者滴加入后者,还是后者滴加前者,都有气体产生,但最终生成的气体积不同,则盐酸的浓度是( )| A. | 1.5mol/L | B. | 2.0mol/L | C. | 1mol/L | D. | 2.5mol/L |
分析 当碳酸钠滴入盐酸中时发生CO32-+2H+═H2O+CO2↑,当盐酸滴入碳酸钠溶液时,发生反应为CO32-+H+═HCO3-、HCO3-+H+═H2O+CO2↑,不管是将前者加入后者中,还是将后者加入前者中,都有气体产生,说明n(HCl):n(Na2CO3)>1:1,但最终产生的气体体积不同,说明n(HCl):n(Na2CO3)<2:1,根据二者之间的关系式来分析解答.
解答 解:当碳酸钠滴入盐酸中时发生CO32-+2H+═H2O+CO2↑,当盐酸滴入碳酸钠溶液时,反应顺序为CO32-+H+═HCO3-、HCO3-+H+═H2O+CO2↑,不管是将前者加入后者中,还是将后者加入前者中,都有气体产生,说明n(HCl):n(Na2CO3)>1:1,但最终产生的气体体积不同,说明n(HCl):n(Na2CO3)<2:1,
所以1<n(HCl):n(Na2CO3)<2,n(Na2CO3)=0.20mol,
则0.2mol<n(HCl)<0.4mol,盐酸的体积是200mL,所以$\frac{0.2mol}{0.2L}$<c(HCl)<$\frac{0.4mol}{0.2L}$,
即1mol/L<c(HCl)<2mol/L,
故选A.
点评 本题考查化学方程式的有关计算,明确二者滴定顺序不同其反应方程式不同是解本题关键,再根据题意结合反应方程式进行计算,注意碳酸钠和稀盐酸反应先后顺序,难度中等.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
15.按要求回答下列有关问题.
(1)据报道,科学家新研发出一种常温下催化合成NH3的方法:N2(g)+6H2O(l)═4NH3(g)+3O2(g)
已知如下信息:
①化合物的生成热可以表示其相对能量.化学上,规定标准状况下稳定单质的生成热为0.几种物质的生成热:NH3(g)为mkJ•mol-1,H2O(l)为nkJ•mol-1.
反应的△H=产物的生成热之和-反应物的生成热之和
②几种化学键的键能数据如下:
上述反应中,△H=4m-6nkJ•mol-1,H-N键的键能为$\frac{2a+12b-3c-4m+6n}{12}$kJ•mol-1.
(2)二氧化硫在一定条件下可以发生如下反应:SO2(g)+NO2(g)?SO3(g)+NO(g),△H=-42kJ•mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)=0.05mol•L-1•min-1;
②实验丙中,达到平衡时,NO2的转化率为$\frac{10a}{3}$×100%;
③由表中数据可推知,Tl<T2(填“>”“<’’或“=”);
(3)对反应N2O4(g)?2NO2(g)△H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图1所示,下列说法正确的是d.

a.A、C两点的反应速率:A>C
b.A、C两点气体的颜色:A深,C浅
c.由状态A到状态B,可以用加热的方法
d.A、C两点的化学平衡常数:A=C
(4)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN-(N为-3价,下同),装置如图2所示,通电过程中,阳极区两种离子的放电产物会进一步发生反应,其方程式为:Cl2+CNO-+OH-→□+Cl-+CO32-+H2O(未配平).最终阴、阳两极均有无色无味气体产生.
①铁电极应连接直流电源的负极(填写电极名称).
②上述反应方程式配平后“□”内应填写N2;
③阳极上发生的电极反应为2Cl--2e-═Cl2↑和CN--2e-+2OH-=CNO-+H2O.
(1)据报道,科学家新研发出一种常温下催化合成NH3的方法:N2(g)+6H2O(l)═4NH3(g)+3O2(g)
已知如下信息:
①化合物的生成热可以表示其相对能量.化学上,规定标准状况下稳定单质的生成热为0.几种物质的生成热:NH3(g)为mkJ•mol-1,H2O(l)为nkJ•mol-1.
反应的△H=产物的生成热之和-反应物的生成热之和
②几种化学键的键能数据如下:
| 化学键 | N≡N | H-O | O-O | H-N |
| E/kJ•mol-1 | a | b | c | d |
(2)二氧化硫在一定条件下可以发生如下反应:SO2(g)+NO2(g)?SO3(g)+NO(g),△H=-42kJ•mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| N(SO2) | N(NO2) | N(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
②实验丙中,达到平衡时,NO2的转化率为$\frac{10a}{3}$×100%;
③由表中数据可推知,Tl<T2(填“>”“<’’或“=”);
(3)对反应N2O4(g)?2NO2(g)△H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图1所示,下列说法正确的是d.

a.A、C两点的反应速率:A>C
b.A、C两点气体的颜色:A深,C浅
c.由状态A到状态B,可以用加热的方法
d.A、C两点的化学平衡常数:A=C
(4)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN-(N为-3价,下同),装置如图2所示,通电过程中,阳极区两种离子的放电产物会进一步发生反应,其方程式为:Cl2+CNO-+OH-→□+Cl-+CO32-+H2O(未配平).最终阴、阳两极均有无色无味气体产生.
①铁电极应连接直流电源的负极(填写电极名称).
②上述反应方程式配平后“□”内应填写N2;
③阳极上发生的电极反应为2Cl--2e-═Cl2↑和CN--2e-+2OH-=CNO-+H2O.
16.在强酸性溶液中能大量共存的无色透明离子组是( )
| A. | Mg2+ Na+ Cl- SO42- | B. | K+ Na+ CO32- NO3- | ||
| C. | K+ Na+ Cl- Cu2+ | D. | Na+Ba2+OH- SO42- |
 ,可使水的电离平衡正向移动的是( )
,可使水的电离平衡正向移动的是( )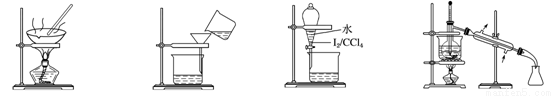
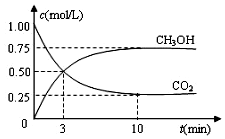 目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.现向体积为1L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.现向体积为1L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.