题目内容
在水中加入下列物质 ,可使水的电离平衡正向移动的是( )
,可使水的电离平衡正向移动的是( )
A.NaOH B.NH4Cl C.NaCl D.H2SO4
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是A(填写物质的序号).
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)为配制500mL上述“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管.(在横线上填写相应仪器的名称),
(3)某同学取用保鲜剂固体配制溶液的过程如图所示,其错误操作序号是①⑤
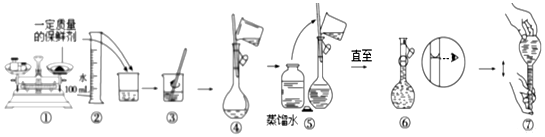
(4)在溶液配制过程中,下列实验操作会使配得的溶液浓度偏大的是AC.
A.溶解固体时,未冷却就直接转移
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)为配制500mL上述“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管.(在横线上填写相应仪器的名称),
(3)某同学取用保鲜剂固体配制溶液的过程如图所示,其错误操作序号是①⑤

(4)在溶液配制过程中,下列实验操作会使配得的溶液浓度偏大的是AC.
A.溶解固体时,未冷却就直接转移
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度.
7.含有0.20mol Na2CO3的溶液120mL和200mL 盐酸,不管将前者滴加入后者,还是后者滴加前者,都有气体产生,但最终生成的气体积不同,则盐酸的浓度是( )
| A. | 1.5mol/L | B. | 2.0mol/L | C. | 1mol/L | D. | 2.5mol/L |



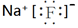 .
. 实验室合成乙酸乙酯如(如图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是(78.5℃、118℃、77.1℃)
实验室合成乙酸乙酯如(如图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是(78.5℃、118℃、77.1℃)
