题目内容
20.下列叙述正确的是( )| A. | 将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | |
| B. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则C1=l0C2 | |
| C. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| D. | NaHCO3溶液中有:HCO3-+H2O?CO32-+H3O+加水稀释后,H+浓度减小 |
分析 A.溶液中存在电荷守恒判断;
B.相同温度下,不同浓度的醋酸溶液,醋酸的浓度越大其电离程度越小;
C.氢氧化钠是强电解质,醋酸是弱电解质,在溶液中存在电离平衡,pH=11的NaOH溶液与pH=3的醋酸溶液中,醋酸浓度大于氢氧化钠,等体积混合酸有剩余;
D.HCO3-+H2O?CO32-+H3O+,为碳酸氢根离子电离方程式,加水稀释后促进碳酸氢根离子水解,氢氧根离子浓度减小,离子积常数判断氢离子浓度增大.
解答 解:A.混合溶液呈中性,所以c(H+)=c(OH-),根据电荷守恒得c(NH4+)+c(H+)=c(OH-)+2c(SO42-),所以c(NH4+)>c(SO42-),故A错误;
B.相同温度下,不同浓度的醋酸溶液,醋酸的浓度越大其电离程度越小,假设电离程度相同时c1=10c2,实际上c1的电离程度小于c1,所以c1>10c2,故B错误;
C.pH=11的NaOH溶液与pH=3的醋酸溶液中,醋酸浓度大于氢氧化钠,等体积混合酸有剩余,溶液呈酸性,石蕊试液遇酸变红色,故C正确;
D.碳酸氢钠溶液中碳酸氢根离子水解溶液显碱性,HCO3-+H2O?CO32-+H3O+,为碳酸氢根离子电离方程式,加水稀释后促进碳酸氢根离子水解,氢氧根离子浓度减小,离子积常数不变,判断氢离子浓度增大,故D错误;
故选C.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点、pH与氢离子浓度的换算、弱电解质电离程度与浓度的关系是解本题关键,易错选项是B,可以采用假设的方法分析解答,题目难度中等.

练习册系列答案
相关题目
10.下列叙述正确的是( )
| A. | 硫酸钡难溶于水,在水溶液中不能导电,所以硫酸钡不是电解质 | |
| B. | 电解质的电离一定要在水分子作用下才能进行 | |
| C. | 三氧化硫溶于水能导电,所以三氧化硫是电解质 | |
| D. | 硫酸、氢氧化钡、纯碱、苛性钠都是电解质 |
11.用惰性电极电解CuSO4溶液一段时间后停止通电,若需向溶液中加入1molCu(OH)2才能使溶液恢复至电解前的状态,则电解过程中转移电子的物质的量为( )
| A. | 2mol | B. | 4mol | C. | 6mol | D. | 8mol |
8.下列有关化学用语表示正确的是( )
| A. | 氯乙烯的结构式:H2C=CHCl | B. | S2-的结构示意图: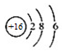 | ||
| C. | 熟石膏的化学式:2CaSO4•H2O | D. | 二氧化碳的比例模型: |
15.液氨与纯水相似,也存在着微弱的电离:2NH3?NH4++NH2-,据此判断以下叙述中错误的是( )
| A. | NH3、NH4+、NH-的电子数相等,化学性质也相同 | |
| B. | 一定温度下液氨中c(NH4+)•c(NH2-)是一个常数 | |
| C. | 液氨的电离达到平衡时c(NH3)≠c(NH4+)=c(NH2-) | |
| D. | 加入其他物质,c(NH4+)/c(NH2-)可能不变 |
5.根据化学反应的实质是旧键断裂,新键形成这一观点,下列变化不属于化学反应的是( )
| A. | 干冰气化 | B. | O2转变成O3 | C. | 加热NH4HCO3 | D. | 加热NaHCO3 |
12.人类第一次获得金属铝是在1825年由丹麦化学家用无水AlCl 3与钾作用制得的,当时由于价格非常昂贵,称为“银色的金子”.直到19世纪后期发明了电解法生产铝,才使铝的价格大大下降,使铝成为当今广泛应用的一种金属材料.下列关于铝的叙述,不正确的是( )
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 在常温下,铝不能与浓硫酸反应 | |
| C. | 铝是一种比较活泼的金属 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
9.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应式为Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A. | 该电池中Zn为负极,发生还原反应 | |
| B. | 该电池的正极反应式为MnO2+e-+H2O=MnOOH+OH- | |
| C. | 导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn | |
| D. | 电池工作时内电路中OH-移动向MnO2一极 |