题目内容
8.设NA为阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA | |
| B. | 物质的量浓度为0.1mol•L-1的MgCl2溶液中,含有Cl-个数为0.2NA | |
| C. | 标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA | |
| D. | 常温下,22g CO2和N2O混合气体中,含有的原子数目为1.5NA |
分析 A、氯气和水的反应为可逆反应;
B、溶液体积不明确;
C、标况下甲醇为液体;
D、CO2和N2O的摩尔质量均为44g/mol.
解答 解:A、氯气和水的反应为可逆反应,故不能进行彻底,故转移的电子数小于0.1NA个,故A错误;
B、溶液体积不明确,故溶液中的氯离子的个数无法计算,故B错误;
C、标况下甲醇为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、CO2和N2O的摩尔质量均为44g/mol,故22g混合物的物质的量为0.5mol,而两者均为三原子分子,故0.5mol混合物中含1.5NA个原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列实验操作正确的是( )
| A. | 蒸发操作时,应将溶液完全蒸干后停止加热 | |
| B. | 稀释浓硫酸时,沿烧杯内壁将浓硫酸缓慢加入水中,边加边搅拌 | |
| C. | 分液操作时,先放出下层液体,再关闭活塞,从漏斗口倒出上层液体 | |
| D. | 配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管吸出多余液体 |
4.下列4组物质的鉴别方法不正确的是( )
| A. | NH4Cl固体和NaCl固体-分别滴加NaOH溶液并加热 | |
| B. | K2SO4固体和Na2SO4固体-焰色反应 | |
| C. | HC1溶液和H2SO4溶液-分别滴加AgNO3溶液 | |
| D. | FeC13溶液和Fe(OH)3胶体一束强光照射 |
16.下列说法正确的是( )
| A. | 烧碱、冰醋酸、四氯化碳均为电解质 | |
| B. | 胆矾、冰水混合物、四氧化三铁都不是混合物 | |
| C. | 分离胶体和某盐溶液,可用过滤的方法 | |
| D. | SO2、SiO2、CO均为酸性氧化物 |
3.101kPa时,S(s)+O2(g)═SO2(g)△H=-297.23kJ•mol-1.据此分析,下列说法中不正确的是( )
| A. | S的燃烧热为297.23 kJ•mol-1 | |
| B. | S升华是吸热过程 | |
| C. | 形成1 mol SO2的化学键释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量 | |
| D. | S(g)+O2(g)═SO2(g)放出的热量小于297.23 kJ |
13.下列有关化学用语表示正确的是( )
| A. | 乙醇的分子式:C2H5OH | B. | C的基态原子核外电子轨道表示式: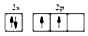 | ||
| C. | 氯化铵的电子式: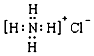 | D. | CS2分子比例(填充)模型: |
18.下列分子的中心原子是sp2杂化的是( )
| A. | CH4 | B. | H2O | C. | PBr3 | D. | BF3 |