题目内容
某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,则下列说法中正确的是( )
| A、混合气体中一定没有乙炔 |
| B、混合气体中一定有乙烯 |
| C、混合气体可能由乙炔和丙烯组成 |
| D、混合气体可能由丙烯和丙炔组成 |
考点:有关混合物反应的计算
专题:计算题
分析:某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,相同条件下,气体的密度之比等于其摩尔质量之比,所以该混合物的相对分子质量为13.5×2=27,则该混合气体中一种物质相对分子质量大于27一种物质相对分子质量小于27,据此分析解答.
解答:
解:某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,相同条件下,气体的密度之比等于其摩尔质量之比,所以该混合物的相对分子质量为13.5×2=27,则该混合气体中一种物质相对分子质量大于27一种物质相对分子质量小于27,乙炔的相对分子质量为26,所有的烯烃和炔烃中只有乙炔的相对分子质量小于27,所以该混合气体中一定含有乙炔,
A.乙炔的相对分子质量为26,所有的烯烃和炔烃中只有乙炔的相对分子质量小于27,所以该混合气体中一定含有乙炔,故A错误;
B.乙烯的相对分子质量为30,该混合气体中一定含有乙炔,所以可能含有乙烯,故B错误;
C.该混合气体中一定含有乙炔,丙烯的相对分子质量为42>27,所以符合条件,故C正确;
D.该混合气体中一定含有乙炔,一定不含丙炔,故D错误;
故选C.
A.乙炔的相对分子质量为26,所有的烯烃和炔烃中只有乙炔的相对分子质量小于27,所以该混合气体中一定含有乙炔,故A错误;
B.乙烯的相对分子质量为30,该混合气体中一定含有乙炔,所以可能含有乙烯,故B错误;
C.该混合气体中一定含有乙炔,丙烯的相对分子质量为42>27,所以符合条件,故C正确;
D.该混合气体中一定含有乙炔,一定不含丙炔,故D错误;
故选C.
点评:本题考查混合物的计算,利用平均摩尔质量采用讨论方法解答,知道相同条件下气体密度与其摩尔质量的关系,题目难度中等.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如下图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的( )
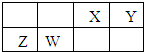

| A、Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B、原子半径由小到大的顺序为:X<Z<Y<W |
| C、与同浓度的盐酸反应,Z比W更剧烈 |
| D、W的金属性比Z的强 |
下列有关物质的性质的说法正确的是( )
| A、金刚石、C60都有较大的硬度和较高的熔点 |
| B、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C、Cl2、SO2都可以使品红溶液褪色 |
| D、镁、铁等金属在一定条件下与水反应都生成对应的氢氧化物和氢气 |
已知甲为恒温、乙为恒压容器.两容器中均充入1molN2、3molH2,初始时两容器的温度、体积相同.一段时间后反应达到平衡,为使两容积中的N2在平衡混合物中的物质的量分数相同,下列措施中不可行的是( )
| A、向甲容器中充入一定量的氦气 |
| B、向乙容器中充入一定量的N2 |
| C、升高乙容器的温度 |
| D、增大甲容器的压强 |

 (酮中R、R′代表烃基且酮不能再被氧化为羧酸,其它物质中R、R′代表烃基或氢原子)
(酮中R、R′代表烃基且酮不能再被氧化为羧酸,其它物质中R、R′代表烃基或氢原子)
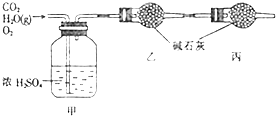
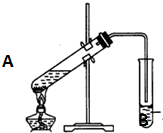 实验室用一定比例的乙醇、乙酸和浓硫酸的混合液制备乙酸乙酯,装置如图所示:
实验室用一定比例的乙醇、乙酸和浓硫酸的混合液制备乙酸乙酯,装置如图所示: