题目内容
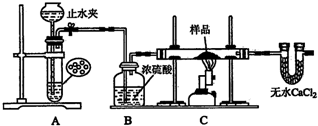
已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过下图所示的装置,得到如下表所示的实验数据(假设生成的气体全部被吸收)
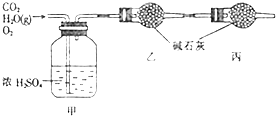
根据实验数据填空:
(1)该燃料完全燃烧生成CO2的质量为 g.
(2)该燃料分子中碳、氢原子的数目比为 .
(3)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为 ,其可能的结构简式为 .

| 实验前 | 实验后 | |
| 甲的质量/g | 101.1 | 103.8 |
| 乙的质量/g | 82.0 | 86.4 |
(1)该燃料完全燃烧生成CO2的质量为
(2)该燃料分子中碳、氢原子的数目比为
(3)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为
考点:有机物实验式和分子式的确定
专题:实验探究和数据处理题
分析:有机物的燃烧试验中,有机物中的碳元素全部转化为二氧化碳,氢元素全部转化为水,浓硫酸增重量即为生成水的质量,碱石灰增加的质量即为二氧化碳的质量,根据碳元素和氢元素守恒来确定有机物的组成和原子数目,结合相对分子质量来确定分子式.
解答:
解:(1)碱石灰可吸收二氧化碳,增加的质量:86.4g-82.0g=4.4g,故答案为:4.4;
(2)有机物燃烧生成水的物质的量为
=0.15mol,有机物燃烧生成二氧化碳的质量为:
=0.1mol,根据元素守恒,则该燃料分子中碳、氢原子的数目比为0.1:0.3=1:3,故答案为:1:3;
(3)该燃料分子的式量为46,每个分子中含有1个氧原子,则碳原子和氢原子的总是量为30,根据碳、氢原子的数目比为3:1,所以碳原子数目为2,氢原子数目为6,其分子式为C2H6O,结构简式为CH3CH2OH(或CH3OCH3),故答案为:C2H6O;CH3CH2OH(或CH3OCH3).
(2)有机物燃烧生成水的物质的量为
| 2.7g |
| 18g/mol |
| 4.4g |
| 44g/mol |
(3)该燃料分子的式量为46,每个分子中含有1个氧原子,则碳原子和氢原子的总是量为30,根据碳、氢原子的数目比为3:1,所以碳原子数目为2,氢原子数目为6,其分子式为C2H6O,结构简式为CH3CH2OH(或CH3OCH3),故答案为:C2H6O;CH3CH2OH(或CH3OCH3).
点评:本题考查有机物实验式和分子式的确定,有机物的燃烧法和元素守恒法是确定有机物分子式的简单方法,注意平时知识的积累是解题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某研究小组为测定食用白醋中醋酸的含量进行的如下操作,正确的是( )
| A、用碱式滴定管量取一定体积的待测白醋放入锥形瓶中 |
| B、称取4.0gNaOH到1000mL容量瓶加水至刻度,配成1.00 mol?L-1NaOH标准溶液 |
| C、用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不退色时,为滴定终点 |
| D、滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量 |
某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,则下列说法中正确的是( )
| A、混合气体中一定没有乙炔 |
| B、混合气体中一定有乙烯 |
| C、混合气体可能由乙炔和丙烯组成 |
| D、混合气体可能由丙烯和丙炔组成 |
现欲粗略测定一未知浓度的醋酸溶液中CH3COOH的电离度,应做的实验和所需的试剂(或试纸)是( )
| A、电解、NaOH溶液 |
| B、蒸馏、Na2CO3溶液 |
| C、酯化反应、石蕊试液 |
| D、中和滴定、pH试纸 |
10月24日“嫦娥一号”发射升空,在三级动力中采用了氢氧燃料.已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A、H2O(g)═H2(g)+
| ||
| B、2H2(g)+O2(g)═2H2O(l)△H=-484kJ?mol-1 | ||
C、H2(g)+
| ||
| D、2H2(g)+O2(g)═2H2O(g)△H=+484kJ?mol-1 |
 某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:
某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下: