题目内容
14.下列关于卤族元素的说法正确的是( )| A. | F、Cl、Br、I最高正化合价都为+7 | |
| B. | 卤族元素的单质只有氧化性 | |
| C. | 从F到I,原子的得电子能力依次减弱 | |
| D. | 卤素单质与H2化合的难易程度按F2、Cl2、Br2、I2的顺序由难变易 |
分析 A、氟无正价;
B、氯气既有氧化性又有还原性,根据卤素单质性质的相似性来回答;
C、同主族从上往下非金属性减弱;
D、元素的非金属性越强,其单质与氢气与容易化合.
解答 解:A、氟无正价,故A错误;
B、氯气既有氧化性又有还原性,可以推知溴、碘单质既有氧化性又有还原性,故B错误;
C、同主族从上往下非金属性减弱,所以从F到I,原子的得电子能力依次减弱,故C正确;
D、元素的非金属性越强,其单质与氢气与容易化合,非金属性F>Cl>Br>I,所以卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难,故D错误;
故选C.
点评 本题考查同一主族元素性质递变规律,侧重考查元素周期律的应用,以卤族元素为例熟练掌握同一周期、同一主族性质递变规律,注意规律中的异常现象,题目难度不大.

练习册系列答案
相关题目
4.某烃X能使溴的CCl4溶液褪色,完全燃烧时1molX需要消耗9molO2且生成等物质的量的CO2与H2O.若其结构中含有两个-CH3,则该物质的结构(不考虑立体异构)最多有( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 7种 |
2.下列对分子性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 由于乳酸( )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 | |
| C. | HF的稳定性很强,是因为其分子间能形成氢键 | |
| D. | 由右图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子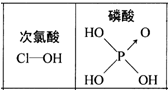 |
9.下列分子中中心原子采取sp2杂化的是( )
| A. | PCl3 | B. | CH4 | C. | BF3 | D. | H2O |
19.下列各组化合物中,属同系物的是( )
| A. | C2H6和C4H8 | B. | C3H6和C6H14 | C. | C8H18和C4H10 | D. | C5H12和C7H14 |
3.下列叙述错误的是( )
| A. | 用AgNO3溶液可以鉴别KCl和KI | |
| B. | SO2使溴水褪色与乙烯使KMnO4溶液褪色原理相同 | |
| C. | 可根据硫酸密度的大小判断铅蓄电池是否需要充电 | |
| D. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
 有机物之间的反应通常比较复杂,同样的反应物在不同条件下生成不同的产物.
有机物之间的反应通常比较复杂,同样的反应物在不同条件下生成不同的产物.