题目内容
12.下列实验的现象与对应结论均正确的是( )| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al浓硝酸不反应 |
| C | 将盐酸滴入NaOH溶液 | 无现象 | 盐酸与氢氧化钠不反应 |
| D | 将水蒸气通过灼热铁粉 | 粉末变红 | 铁水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体;
B.常温下浓硫酸、浓硝酸遇到铝、铁发生钝化现象,生成一薄层致密的氧化物薄膜阻止反应进行;
C.盐酸与氢氧化钠溶液发生中和反应,反应现象不明显;
D.铁在高温条件与水反应生成四氧化三铁黑色固体.
解答 解:A.将浓硫酸滴到蔗糖表面,固体变黑膨胀,浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体表现浓硫酸的氧化性,故A正确;
B.常温下将Al片放入浓硝酸中,无明显变化,铝和浓硝酸发生钝化现象,发生反应生成一薄层致密的氧化物薄膜阻止反应进行,表现了强氧化性,故B错误;
C.向盐酸中滴加氢氧化钠溶液,没有明显的反应现象,但是二者反应生成了水和氯化钠,故C错误;
D.将水蒸气通过灼热的铁粉,反应生成黑色的四氧化三铁固体,说明铁在高温下和水反应,不是生成氧化铁,故D错误;
故选A.
点评 本题考查了浓硫酸、浓硝酸等物质的性质,题目难度不大,注意掌握浓硫酸、浓硝酸具有的性质,明确铝、铁在常温下与浓硫酸、浓硝酸发生了钝化现象,不是不反应,为易错点.

练习册系列答案
相关题目
5. 磷酸吡醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如图,下列有关叙述不正确的是( )
磷酸吡醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如图,下列有关叙述不正确的是( )
 磷酸吡醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如图,下列有关叙述不正确的是( )
磷酸吡醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如图,下列有关叙述不正确的是( )| A. | 该物质的分子式为C8H9O6NP | |
| B. | 该物质能与金属钠反应,能发生银镜反应,还能使石蕊试液变红 | |
| C. | 作为芳香族化合物,该物质可能具有芳香气味 | |
| D. | 1mol该酯与NaOH溶液反应,最多消耗3mol NaOH |
3. 某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究.
某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究.
【提出假设】:
小组同学经过分析讨论认为生成气体可能含H2和SO2.
【设计实验方案,验证假设】主要包括两个环节:
Ⅰ.验证SO2,实验装置如图所示;
Ⅱ.检验产物中含有H2,实验内容将由B部分导出的气体依次通过装置C、D、E、F、G.Ⅱ中装置C、D、E、F、G的信息如表所示:
试回答下列问题:
(1)小组同学认为生成气体中含H2的理由是随着反应的进行,硫酸的浓度变小;
(2)盛放锌粒的仪器名称是蒸馏烧瓶;
(3)B部分装置的目的是验证SO2并探究SO2与品红作用的可逆性,实验的操作及主要现象是品红溶液先褪色,加热后又恢复红色;
(4)①装置D、G的作用依次是干燥H2,防止干扰后面H2的检验、防止空气中的水蒸气进入H;
②E中发生反应的化学方程式是CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
③试剂X是无水CuSO4粉末.
 某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究.
某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究.【提出假设】:
小组同学经过分析讨论认为生成气体可能含H2和SO2.
【设计实验方案,验证假设】主要包括两个环节:
Ⅰ.验证SO2,实验装置如图所示;
Ⅱ.检验产物中含有H2,实验内容将由B部分导出的气体依次通过装置C、D、E、F、G.Ⅱ中装置C、D、E、F、G的信息如表所示:
| 仪器标号 | C | D | E | F | G |
| 仪器 | 洗气瓶 | 洗气瓶 | 硬质玻璃管,加热 | 干燥管 | 干燥管 |
| 仪器中所加物质 | NaOH溶液 | 浓硫酸 | CuO粉末 | 试剂X | 无水CaCl2固体 |
(1)小组同学认为生成气体中含H2的理由是随着反应的进行,硫酸的浓度变小;
(2)盛放锌粒的仪器名称是蒸馏烧瓶;
(3)B部分装置的目的是验证SO2并探究SO2与品红作用的可逆性,实验的操作及主要现象是品红溶液先褪色,加热后又恢复红色;
(4)①装置D、G的作用依次是干燥H2,防止干扰后面H2的检验、防止空气中的水蒸气进入H;
②E中发生反应的化学方程式是CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
③试剂X是无水CuSO4粉末.
20.一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
| A. | 以X浓度变化表示的反应速率为0.001 mol/(L•s) | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 其他条件不变时,若增大压强,则物质Y的转化率减小 | |
| D. | 其他条件不变时,若升高温度,X的体积分数增大,则该反应的△H>0 |
7.A、B两元素为某周期ⅡA族和ⅢA族元素,若A元素的原子序数为m,则B元素的原子序数可能为
①m+1 ②m+81 ③m+11 ④m+18 ⑤m+25 ⑥m+32( )
①m+1 ②m+81 ③m+11 ④m+18 ⑤m+25 ⑥m+32( )
| A. | ①③⑥ | B. | ①③⑤ | C. | ②④⑤ | D. | ①②④⑥ |
17.填写下表:
| 类 别 | 典型代表物名称 | 官能团名称 | 结构简式 |
| 醇 | 乙醇 | 羟基 | CH3CH2OH |
| 酚 | 苯酚 | 羟基 |  |
| 醛 | 乙醛 | 醛基 | CH3CHO |
| 羧酸 | 乙酸 | 羧基 | CH3COOH |
4.将三种黑色粉末组成的混和物加入到100mL 14mol/L某热浓酸中,充分反应后得到蓝绿色溶液和两种气体;将从蓝绿色溶液中分离得到的盐与0.15mol还原铁粉恰好反应完全,可得浅绿色溶液和6.4g红色沉淀;将上述生成的两种气体通入足量饱和NaHCO3溶液中,仍然收集到两种气体,据此推断黑色粉末可能为( )
| A. | 物质的量 FeS:CuO:Fe=1:1:1 | |
| B. | 物质的量 C:CuO:Fe=3:2:2 | |
| C. | 质量 MnO2:CuO:C=5.5:8:1.2 | |
| D. | 质量 Fe:C:CuO=7:5:3 |
1.下列离子方程式正确的是( )
| A. | 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ | |
| B. | CuSO4与Ba (OH)2溶液混合 Cu2++SO42-+2OH-+Ba2+=BaSO4↓+Cu(OH)2↓ | |
| C. | 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-=CaCO3↓ | |
| D. | 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |
2.下列有关氧气的实验,正确的是( )
| A. |  制取氧气 | B. | 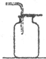 收集氧气 | ||
| C. | 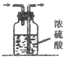 干燥氧气 | D. |  铁丝在氧气中燃烧 |